2. 中国科学院昆明植物研究所山地生态系统研究中心 昆明 650201;
3. 中国科学院大学 北京 100049;
4. 中国农业科学院蜜蜂研究所农业部授粉昆虫生物学重点实验室 北京 100093
2. Centre for Mountain Ecosystem Studies, Kunming Institute of Botany, Chinese Academy of Sciences, Kunming 650201, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China;
4. Key Laboratory for Insect-Pollinator Biology of the Ministry of Agriculture, Institute of Apicultural Research, Chinese Academy of Agricultural Sciences, Beijing 100093, China
传粉服务 (pollination service) 是生态系统的重要功能, 揭示生态系统传粉服务功能维持机制是当前研究的热点[1-2]。普遍的观点认为, 响应多样性 (response diversity) 对维持生态系统传粉稳定性具有重要的作用[3-5]。该理论指出, 生态系统内不同传粉者对环境胁迫响应特征、过程和尺度在时空上存在差异, 从而保障生态系统传粉服务稳定性[3, 6]。由此可见, 探索传粉者对环境胁迫响应规律具有重要的科学和生态意义。
研究表明, 生境丧失是传粉蜂受到的主要胁迫, 其中以自然半自然生境减少为主要表现形式[7-8]。已有的研究从局部尺度和景观尺度下揭示了自然半自然生境减少对传粉蜂的影响。从局部尺度上来看, 邻近自然半自然生境传粉蜂多样性高, 而远离自然半自然生境传粉蜂多样性降低[9]。从景观尺度来看, 自然半自然生境数量降低引起传粉蜂多样性下降[2, 10]。同时, 不同传粉者对自然半自然生境变化的响应过程存在差异[11-12]。比如, 除蜜蜂 (Apis spp.) 外的野生蜂多样性随自然半自然生境数量的减少而下降时, 蜜蜂数量 (含人工饲养蜜蜂) 并不随之减少[13-14]。
我国野生传粉昆虫多样性十分丰富[15]。欧美等地农林生态系统传粉昆虫多样性及影响因素的研究相对较多, 而我国相关研究十分缺乏, 对重要农林生态系统传粉服务功能维持机制认识不清楚[16-18]。理论和研究方面的缺失可能影响传粉昆虫保护, 甚至可能关系到粮食供给的安全性。因而, 有必要对特定农林生态系统开展研究, 了解传粉蜂多样性特征、受到的环境胁迫以及引起的传粉服务功能变化动态[18]。
云贵高原是我国野生蜂最丰富的区域之一。前期研究表明, 该区域野生蜂 (如熊蜂Bumbus spp.) 因自然半自然生境丧失而多样性下降, 引起部分生态系统传粉服务功能不足[14, 19]。作为野生蜂多样性热点区域, 传粉蜂受到的胁迫、强度以及它们对生境丧失的响应规律目前还不清楚。本研究以滇东南岩溶地貌下南瓜 (Cucurbita moschata Duch.) 农田生态系统及其传粉昆虫为对象, 探索优势传粉者蜜蜂密度和熊蜂密度对农田景观中自然半自然生境数量变化和离自然半自然生境距离的响应特征, 为揭示我国云贵高原生态系统传粉服务功能稳定性奠定基础。
1 材料与方法 1.1 样地选择试验于2015年6—7月中旬在云南省文山州广南县 (图 1A, 23°47'~24°20'N, 104°34'~105°22'E) 进行, 选择18个南瓜样地, 其中8个样地用于研究南瓜传粉昆虫群落组成对农田景观的响应规律 (简称“景观作用”), 12个样地用于研究南瓜样地离自然半自然生境不同距离下传粉昆虫群落组成变化 (简称“距离作用”, 其中2样地同时用于研究“景观作用”和“距离作用”, 图 1B-C)。为研究“景观作用”对南瓜传粉蜂群落组成的影响, 根据样地周围自然半自然生境 (次生林+草地, 见“景观分析”部分) 数量变化梯度 (0~91.40%) 选择南瓜样地 (图 1B)。为确保样地空间独立性, 各样地间两两距离至少大于5 km。为研究“距离作用”对南瓜传粉昆虫群落组成的影响, 选择离自然半自然生境距离变化梯度 (0~2.55 km: 0表示紧临自然半自然生境, 2.55 km为研究区域离自然半自然生境最远距离) 的南瓜样地进行试验 (图 1C)。南瓜样地面积497~1 604 m2, 由田间种植情况确定。田间抽样时南瓜均处于盛花期。南瓜样地从种植至收获期间未使用农药或除草剂。即使周边作物可能使用农药或杀虫剂以控制病虫害, 但抽样时未发现南瓜样地和周边农田使用农药。

|
图 1 研究区域的地理位置和南瓜样地空间分布 Figure 1 Geographical location of the study region and spatial distribution of the squash fields (dots) in Guangnan, Wenshan A:广南县 (灰色区域) 位于云南省的地理位置; B:广南县境内研究景观作用对南瓜传粉蜂群落组成变化的8个南瓜样地 (圆点); C:研究离自然半自然生境不同距离的样地传粉蜂群落组成变化的12个南瓜样地 (圆点)。A: the location of Guangnan County (gray area) in Yunnan; B: eight quash fields (dots) selected to study the response of pollinator communities to landscape; C: 12 squash fields (dots) selected to study the responses of pollinator communities to distances away from natural and semi-natural habitats. |
根据南瓜样地面积大小, 于样地内设置1个100 m× 3 m的样带, 或者2个50 m×3 m的样带。样带离南瓜地边缘至少5 m。于样带内随机设置20个1 m2的小样方, 各样方相距至少2 m。观察者于小样方中心点观察记录样方内传粉蜂物种及数量。每个样方观察2 min, 因而每个样地观察时间共40 min。于观察期内, 样方内访花昆虫主要有蜜蜂、熊蜂、胡蜂 (Hymenoptera: Vespidae) 和蚂蚁 (Hymenoptera: Formicidae)。胡蜂数量极少, 飞行于花间搜索和捕食其他昆虫, 较少接触花朵, 难于起到传粉作用。在少数花上可观察到蚂蚁访花。由于南瓜雌雄花分离, 研究者未观察到蚂蚁在雌雄花间移动, 因而其传粉作用较弱。蜜蜂和熊蜂是南瓜主要传粉者, 因而观察者记录样方内蜜蜂和熊蜂物种数量和多度。在2 min观察期内, 观察者同时记录飞入样方内的传粉蜂; 样方内的传粉蜂飞离样方, 则观察者不再记录该访花者。熊蜂主要有B. montivagus、B. breviceps、B. atrips和B. ignitus。虽然B. montivagus和B. breviceps分属于Megabombus和Alpigenobombus亚属, 由于B. montivagus和B. breviceps体色 (color pattern) 相似, 难于田间区别, 所以计为montivagus+ breviceps。样方观察后在每个南瓜样地进行至少10 min的田间采集, 发现样地内熊蜂B. montivagus和B. breviceps同时存在。蜜蜂以东方蜜蜂Apis cerana为主, 仅少数访花者为A. mellifera.
1.3 景观分析采用最大似然法解译2009年5月20日的ETM+航空影像 (云量低于3%)。将土地类型划分为6类:次生林、草地、旱地、水田 (包括水浇地)、建筑物 (包括公路) 和水体。兴趣点来源于野外田间采集的样点, 不同类型兴趣点两两间光谱值分离度均高于1.80, 提取数据精度高于94.38%, 适合空间数据分析要求。
不同传粉蜂对景观结构的响应尺度不同, 因而先分析蜜蜂和熊蜂对景观结构的相关性, 再分析在最大相关性下蜜蜂和熊蜂对景观结构的响应规律。分别计算以南瓜样地为中心, 250 m、500 m、750 m、1 000 m 1 500 m、2 000 m和2 500 m空间尺度的圆内“次生林+草地”(自然半自然生境) 和“旱地+水田”(耕地) 面积同所有类型土地面积的比率 (图 2)。在地理信息系统软件下, 设定不同空间尺度的圆缓冲区。在不同尺度的缓冲圆内, 分别计算6类型土地面积以及“次生林+草地”面积和同所有类型土地面积的比率, 从而获得自然半自然生境百分率 (图 2A)。以耕地面积同所有类型土地面积的比率计算耕地面积百分率 (图 2B)。已有的研究表明, 生态系统中野生蜂多样性同自然半自然生境数量存在正相关关系, 而同耕地数量存在负相关关系[20]。通过建立不同类型土地面积百分率同传粉蜂密度间的关系, 探索传粉蜂同自然半自然生境和耕地面积相关性, 并基于最大相关性下计算传粉蜂对自然半自然生境和耕地的响应规律。

|
图 2 以南瓜样地为中心的7个空间尺度 (250~2 500 m) 下自然半自然生境 (A) 和耕地 (B) 面积百分率计算过程 Figure 2 Methods used to calculate the area percentages of natural and semi-natural habitats (A) and farmlands (B) surrounding squash fields at 7 spatial scales (250-2 500 m) |
南瓜样地面积同自然半自然生境百分率不存在显著性相关关系 (所有尺度下r < 0.33, Pearson相关性检验P > 0.42), 同耕地面积也不存在显著性相关关系 (所有尺度下|r| < 0.41, Pearson相关性检验的P > 0.31), 表明空间南瓜样地面积不随景观结构变化而变化。
1.4 统计分析由Pearson相关系数分别计算熊蜂密度和蜜蜂密度在不同空间尺度下对自然半自然生境和农田的相关性, 并检验相关性是否同零假设 (零相关系数) 存在显著差异。同时, 用Pearson相关系数判定不同空间尺度下自然半自然生境面积百分率同农田面积百分率相关性。
简单线性回归模型 (linear model, LM) 检验南瓜样地面积 (squash field size, FS)、景观中自然半自然生境百分率 (proportion of natural and semi-natural habitats, PNSH) 或耕地百分率 (proportion of farmlands, PF) 对熊蜂密度和蜜蜂密度的影响。同时, 利用简单线性回归模型检验距自然半自然生境的距离和耕地面积对熊蜂密度和蜜蜂密度的影响。构建4备选模型: (1)Y=X1+X2; (2)Y=X1; (3)Y=X2; (4)Y=X1+X2+X1×X2, 式中, X1为样地面积 (FS), X2为自然半自然生境百分率 (PNSH) 或耕地百分率 (PF)。将熊蜂密度和蜜蜂密度对数转换以满足方差齐性和残差正态性。依据低AICc值从备选模型中选择最优模型。由最优模型判定自然半自然生境百分率或南瓜样地面积对熊蜂密度和蜜蜂密度的影响, P < 0.05认为因变量存在显著作用。当部分最优模型不包含样地面积变量时, 或不包含样地面积同自然半自然生境百分率的交互作用时, 我们再结合模型1或模型4进行检验, 进一步判定被最优模型排除的解释变量对因变量的作用。检验结果表明, 不在最优模型中的解释变量不对因变量产生显著影响, 从而证明模型的合理性。
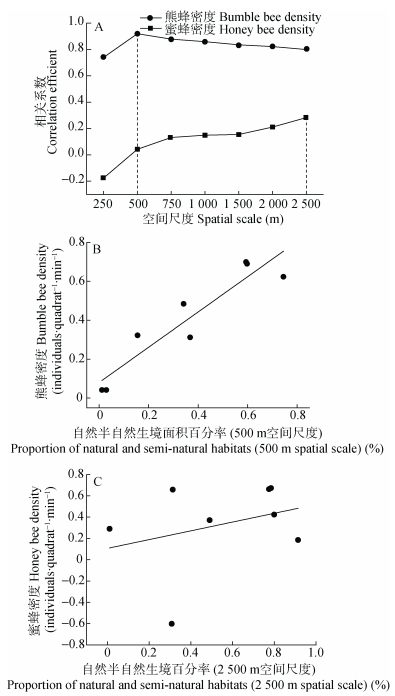
2 结果与分析 2.1 蜜蜂和熊蜂密度对景观中自然半自然生境的响应差异熊蜂密度同自然半自然生境百分率在500 m尺度下显著相关 (t=5.77, df=6, P=0.001);在相关性最强的2 500 m空间尺度下, 未检测到蜜蜂密度同自然半自然生境百分率显著性相关 (t=0.72, df=6, P=0.50)(图 3A)。在500 m尺度下, 熊蜂密度随自然半自然生境百分率的增加而显著增加 (图 3B, 表 1); 在2 500 m尺度下, 蜜蜂密度不随自然半自然生境百分率的增加而显著增加 (图 3C, 表 1)。
|
图 3 同空间尺度下 (250~2 500 m) 熊蜂密度和蜜蜂密度同自然半自然生境百分率相关系数 (A) 以及最大相关系数下熊蜂 (B) 和蜜蜂密度 (C) 对自然半自然生境百分率响应规律 Figure 3 Correlation coefficients between bumble bee density, honey bee density and the area percentages of natural and semi-natural habitats at different spatial scales (A) and responses of bumble bee density (B) and honey bee density (C) to area percentage of natural and semi-natural habitats at the spatial scale with the highest correlation coefficients |
| 表1 南瓜样地面积和自然半自然生境百分率对熊蜂密度和蜜蜂密度的最优线性模型检验拟合结果1) Table 1 Results of the best linear models exploring the effects of patch size of squash field, area percentage of natural and semi-natural habitats and their two-way interactions on bumblebee density and honeybee density1) |
耕地面积百分率同自然半自然生境面积百分率在250 m的空间尺度上不存在显著相关性 (P=0.13), 两者在大于250 m空间尺度时均显著性负相关 (P < 0.05)。
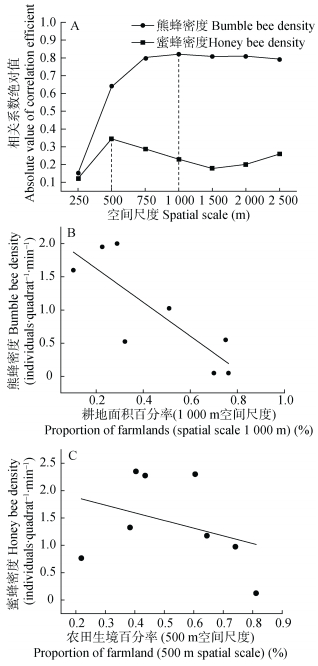
熊蜂密度同景观中耕地面积百分率在1 000 m尺度下显著相关 (t=-3.52, df=6, P=0.01);在相关性最强的500 m空间尺度下, 未检测到蜜蜂密度同自然半自然生境百分率显著联系 (t=-0.90, df=6, P=0.40) (图 4)。在1 000 m尺度下, 熊蜂密度随耕地面积百分率的增加而显著减少 (图 4B, 表 2); 在500 m尺度下, 蜜蜂密度不随耕地面积百分率的增加而显著减少 (图 4C, 表 2)。
|
图 4 不同空间尺度下 (250~2 500 m) 熊蜂密度和蜜蜂密度同耕地面积百分率相关系数 (A) 以及最大相关系数下熊蜂密度 (B) 和蜜蜂密度 (C) 对耕地面积百分率响应规律 Figure 4 Correlation coefficients between bumble bee density, honey bee density and area percentage of farmlands at 250-2 500 m scales (A) and the responses of bumble bee density (B) and honey bee density (C) to area percentage of farmlands at the spatial scale with the highest correlation coefficients |
| 表2 南瓜样地面积和耕地面积百分率对熊蜂密度和蜜蜂密度的最优简单线性模型检验拟合结果1) Table 2 Results of the best linear models exploring the effects of patch size of squash field, area percentage of farmlands and their two-way interactions on bumblebee density and honeybee density1) |
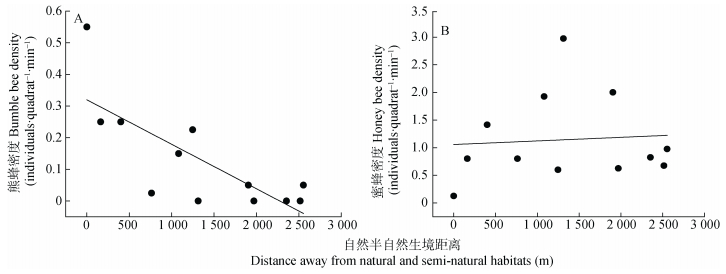
自然半自然生境的距离显著影响熊蜂密度, 但对蜜蜂密度不存在显著影响 (表 3)。距自然生境的距离越大, 熊蜂密度越低 (图 5A), 但蜜蜂密度没有显著性变化 (图 5B)。
| 表3 南瓜样地面积和自然半自然生境的距离对熊蜂密度和蜜蜂密度的简单线性模型拟合结果1) Table 3 Summary of general linear models exploring the effects of patch size of squash field, distance to natural and semi-natural habitats and their two-way interactions on bumble bee density and honey bee density1) |
|
图 5 熊蜂密度 (A) 和蜜蜂密度 (B) 随自然半自然栖境距离的响应规律 Figure 5 Responses of honey bee density (A) and bumble bee density (B) to the distance away from natural and semi-natural habitats |
熊蜂和蜜蜂是滇东南南瓜主要传粉昆虫, 但它们对生境丧失的响应规律存在差异, 首先表现为它们同景观中自然半自然生境的相关性不同。熊蜂密度在500 m空间尺度下对自然半自然生境面积百分率的相关系数最大, 但蜜蜂密度在2 500 m的尺度下对自然半自然生境面积百分率的相关系数最大。此外, 熊蜂密度在1 000 m空间尺度下同耕地面积百分率相关系数最大, 但蜜蜂密度在500 m空间尺度下同耕地面积百分率相关系数最大。已有的研究表明传粉蜂空间响应尺度可能同传粉蜂大小和空间搜索范围相关[12, 21]。然而, 本试验的农田生态系统中蜜蜂密度受人工饲养蜂群数量的干扰, 因而其同自然半自然生境和耕地的关系可能受到影响。
其次, 在最大相关系数对应的空间尺度下, 熊蜂密度和蜜蜂密度对景观中自然半自然生境响应规律存在差异。熊蜂密度随景观中自然半自然生境面积百分率的减少而下降, 而蜜蜂密度随自然半自然生境面积百分率变化不明显。滇东南南瓜传粉熊蜂为野生蜂, 自然半自然生境可为熊蜂提供丰富蜜粉源植物, 因而熊蜂密度受限于自然半自然生境数量。然而, 蜜蜂可能来源于野生蜂群, 也可能来源于人工饲养峰群。由于人工饲养蜜蜂种群数量并不受自然半自然生境的影响, 所以当熊蜂密度随自然半自然生境面积的减少下降时, 蜜蜂密度并不受自然半自然生境面积的影响。
滇东南农田生态系统中, 熊蜂密度同耕地面积百分率显著负相关, 表明景观中耕地面积扩张引起熊蜂下降。滇东南是云南省农产品主要生产区。我们的研究证实农业活动引起该区域熊蜂数量下降, 这与其他农田生态系统已有的研究结果相似, 共同揭示了土地利用类型转换对野生熊蜂多样性的影响[22-23]。农业耕作活动改变景观结构, 将自然半自然生境转换成耕地, 降低了野生传粉蜂的食物资源和筑巢资源, 驱动传粉蜂多样性下降[24]。同时, 农药和除草剂等化学物也可以对野生传粉蜂繁育和种群维持产生负面作用[25]。已有的研究表明, 这些农业耕作活动可能同时发生作用, 共同降低野生熊蜂种群数量[23]。然而值得注意的是, 研究区域农业耕地多分布于岩溶地貌的洼地, 而峰丛的土地石漠化严重, 不易耕种经济作物, 难于转化成农业耕地。因而, 岩溶地貌峰丛多处于自然半自然状态, 可为野生蜂提供必要的食物资源和筑巢资源。虽然我们的研究表明农业耕作活动引起熊蜂多度下降, 但这种下降的强度、范围、变化趋势以及后果需要进一步研究。
离自然半自然生境的距离同样影响熊蜂密度。研究发现离自然半自然距离越远, 熊蜂密度越低, 这与其他研究者发现的规律相似[9, 22]。“距离作用”对熊蜂密度的影响同样可以理解成生境丧失的一种表现形式, 远距离地点野生熊蜂的自然半自然生境降低, 从而导致熊蜂密度下降[12, 26]。虽然“距离作用”显著降低熊蜂密度, 但其对蜜蜂密度的影响作用却不明显。我们认为, 同景观过程相似, 远距离地点的人工饲养蜜蜂同样是干扰蜜蜂密度对距离作用响应过程的重要因素。
研究发现熊蜂密度随生境丧失下降时, 蜜蜂密度并不受生境丧失的影响。熊蜂和蜜蜂对生境丧失的差异性响应具重要的生态学意义。功能冗余的熊蜂和蜜蜂是滇东南南瓜重要的传粉昆虫, 为南瓜提供传粉服务。其他生态系统的研究表明, 熊蜂比蜜蜂具更高的单花柱头花粉沉积量[14, 27]。然而, 熊蜂种群数量易于受景观结构的影响, 其种群数量随生境丧失而下降。庆幸的是, 具有同样传粉功能的蜜蜂密度并不随自然半自然生境的影响。因而, 当熊蜂密度下降时, 蜜蜂访花可以填补熊蜂下降引起的传粉减少, 从而保障生态系统传粉功能维持在一定程度范围内。由此可见, 滇东南熊蜂和蜜蜂对生境丧失的差异性响应规律可能是保障生态传粉服务功能的重要机制, 使生态系统传粉服务功能受到干扰时呈现出一定弹性。然而, 滇东南传粉蜂对土地利用类型转化的响应多样性如何保障南瓜传粉服务需要更深入的研究。
| [1] | Costanza R, d'Arge R, Groot R D, et al. The value of the world's ecosystem services and natural capital[J]. Nature, 1997, 387(6630): 253–260. DOI:10.1038/387253a0 |
| [2] | Kremen C, Williams N M, Aizen M A, et al. Pollination and other ecosystem services produced by mobile organisms:A conceptual framework for the effects of land-use change[J]. Ecology Letters, 2007, 10(4): 299–314. DOI:10.1111/ele.2007.10.issue-4 |
| [3] | Elmqvist T, Folke C, Nyström M, et al. Response diversity, ecosystem change, and resilience[J]. Frontiers in Ecology and the Environment, 2003, 1(9): 488–494. DOI:10.1890/1540-9295(2003)001[0488:RDECAR]2.0.CO;2 |
| [4] | Peterson G, Allen C R, Holling C S. Ecological resilience, biodiversity, and scale[J]. Ecosystems, 1998, 1(1): 6–18. DOI:10.1007/s100219900002 |
| [5] | Winfree R. Global change, biodiversity, and ecosystem services:What can we learn from studies of pollination[J]. Basic and Applied Ecology, 2013, 14(6): 453–460. DOI:10.1016/j.baae.2013.07.004 |
| [6] | Cariveau D P, Winfree R. Causes of variation in wild bee responses to anthropogenic drivers[J]. Current Opinion in Insect Science, 2015, 10: 104–109. DOI:10.1016/j.cois.2015.05.004 |
| [7] | Potts S G, Biesmeijer J C, Kremen C, et al. Global pollinator declines:Trends, impacts and drivers[J]. Trends in Ecology & Evolution, 2010, 25(6): 345–353. |
| [8] | Winfree R, Bartomeus I, Cariveau D P. Native pollinators in anthropogenic habitats[J]. Annual Review of Ecology, Evolution, and Systematics, 2011, 42(1): 1–22. DOI:10.1146/annurev-ecolsys-102710-145042 |
| [9] | Ricketts T H. Tropical forest fragments enhance pollinator activity in nearby coffee crops[J]. Conservation Biology, 2004, 18(5): 1262–1271. DOI:10.1111/cbi.2004.18.issue-5 |
| [10] | Ricketts T H, Regetz J, Steffan-Dewenter I, et al. Landscape effects on crop pollination services:Are there general patterns?[J]. Ecology Letters, 2008, 11(5): 499–515. DOI:10.1111/j.1461-0248.2008.01157.x |
| [11] | Cariveau D P, Williams N M, Benjamin F E, et al. Response diversity to land use occurs but does not consistently stabilise ecosystem services provided by native pollinators[J]. Ecology Letters, 2013, 16(7): 903–911. DOI:10.1111/ele.12126 |
| [12] | Klein A M, Cunningham S A, Bos M, et al. Advances in pollination ecology from tropical plantation crops[J]. Ecology, 2008, 89(4): 935–943. DOI:10.1890/07-0088.1 |
| [13] | Garibaldi L A, Steffan-Dewenter I, Winfree R, et al. Wild pollinators enhance fruit set of crops regardless of honey bee abundance[J]. Science, 2013, 339(6127): 1608–1611. DOI:10.1126/science.1230200 |
| [14] | Xie Z, An J. The effects of landscape on bumblebees to ensure crop pollination in the highland agricultural ecosystems in China[J]. Journal of Applied Entomology, 2014, 138(8): 555–565. DOI:10.1111/jen.2014.138.issue-8 |
| [15] |
徐环李, 杨俊伟, 孙洁茹.
我国野生传粉蜂的研究现状与保护策略[J]. 植物保护学报, 2009, 36(4): 371–376.
Xu H L, Yang J W, Sun J R. Current status on the study of wild bee-pollinators and conservation strategies in China[J]. Acta Phytophylacica Sinica, 2009, 36(4): 371–376. |
| [16] | Teichroew J L, Xu J C, Ahrends A, et al. Is China's unparalleled and understudied bee diversity at risk?[J]. Biological Conservation, 2016. DOI:10.1016/j.biocon.2016.05.023 |
| [17] |
田瑜, 兰存子, 徐靖, 等.
IPBES框架下的全球传粉评估及我国对策[J]. 生物多样性, 2016, 24(9): 1084–1090.
Tian Y, Lan C Z, Xu J, et al. Assessment of pollination and China's implementation strategies within the IPBES framework[J]. Biodiversity Science, 2016, 24(9): 1084–1090. DOI:10.17520/biods.2016138 |
| [18] |
谢正华, 徐环李, 杨璞.
传粉昆虫物种多样性监测、评估和保护概述[J]. 应用昆虫学报, 2011, 48(3): 746–752.
Xie Z H, Xu H L, Yang P. Notes on monitoring, assessing and conserving pollinator biodiversity[J]. Chinese Journal of Applied Entomology, 2011, 48(3): 746–752. |
| [19] |
杨大荣.
云南澜沧江流域传粉昆虫——熊蜂多样性现状与保护对策[J]. 生物多样性, 1999, 7(3): 170–174.
Yang D R. The status of species diversity and conservation strategy of bumble bees, a pollination insect in Lancang River Basin of Yunnan, China[J]. Chinese Biodiversity, 1999, 7(3): 170–174. |
| [20] | Steffan-Dewenter I, Münzenberg U, Bürger C, et al. Scale-dependent effects of landscape context on three pollinator guilds[J]. Ecology, 2002, 83(5): 1421–1432. DOI:10.1890/0012-9658(2002)083[1421:SDEOLC]2.0.CO;2 |
| [21] | Greenleaf S S, Williams N M, Winfree R, et al. Bee foraging ranges and their relationship to body size[J]. Oecologia, 2007, 153(3): 589–596. DOI:10.1007/s00442-007-0752-9 |
| [22] | Klein A M, Vaissière B E, Cane J H, et al. Importance of pollinators in changing landscapes for world crops[J]. Proceedings of the Royal Society B:Biological Sciences, 2007, 274(1608): 303–313. DOI:10.1098/rspb.2006.3721 |
| [23] | Winfree R, Aguilar R, Vázquez D P, et al. A meta-analysis of bees' responses to anthropogenic disturbance[J]. Ecology, 2009, 90(8): 2068–2076. DOI:10.1890/08-1245.1 |
| [24] | Roulston T H, Goodell K. The role of resources and risks in regulating wild bee populations[J]. Annual Review of Entomology, 2011, 56(1): 293–312. DOI:10.1146/annurev-ento-120709-144802 |
| [25] | Goulson D, Nicholls E, Botías C, et al. Bee declines driven by combined stress from parasites, pesticides, and lack of flowers[J]. Science, 2015, 347(6229): 1255957. DOI:10.1126/science.1255957 |
| [26] | Tscharntke T, Klein A M, Kruess A, et al. Landscape perspectives on agricultural intensification and biodiversityecosystem service management[J]. Ecology Letters, 2005, 8(8): 857–874. DOI:10.1111/ele.2005.8.issue-8 |
| [27] | Artz D R, Nault B A. Performance of Apis mellifera, Bombus impatiens, and Peponapis pruinosa (Hymenoptera:Apidae) as pollinators of pumpkin[J]. Journal of Economic Entomology, 2011, 104(4): 1153–1161. DOI:10.1603/EC10431 |
 2017, Vol. 25
2017, Vol. 25



