低温是农业生产中常见的一种严重自然灾害, 它可以使植物细胞脱水、结晶, 原生质内发生不可逆的凝胶化, 造成植物细胞的机械损害或死亡。相对于甘蓝型油菜 (Brassica napus), 白菜型油菜 (Brassica campestris) 具有抗寒性强、耐瘠薄等优良性状, 在北方寒旱区有着甘蓝型油菜无法替代的作用[1]。自孙万仓等[2]提出冬油菜向我国北方寒旱区北移的可行性后, 冬油菜的种植面积日益扩增, 产生了巨大的生态效益和经济效益。冬油菜的成功北移, 主要依赖于超强抗寒品种的成功选育。陇油系列白菜型冬油菜品种抗寒性优异, 但其抗寒机理尚不完全清楚。目前, 对白菜型冬油菜的研究主要集中在其抗寒性的形态特征与生理特征[3]、抗寒响应相关的基因克隆[4-6]等方面, 但是对其抗寒机制的蛋白质组学研究甚少。目前, 蒲媛媛[7]仅在蛋白质上样量的比较和等电聚焦 (IEF) 的优化方面作了初步研究, 尚未对低温胁迫前后的差异蛋白作深入的探究。
蛋白质是生理功能的执行者, 是生命现象的直接体现者。因此, 要对生命的复杂活动有全面和深入的认识, 就必须进行蛋白质组学方面的研究[8]。目前, 双向凝胶电泳 (two-dimensional gel electrophoresis, 2-DE) 技术已成为蛋白质组学研究的首选技术, 特别是用于抗逆性差异蛋白质的分析及鉴定, 利用2-DE技术能够比较分析生物样品在不同条件下蛋白质组学的动态变化, 从而筛选和鉴定出功能特异性的蛋白质及对应的基因。近年来, 2-DE技术被广泛应用于农业、医学和微生物学等领域[9-11]。例如, 崔宇鹏等[12]对盐胁迫下的棉花 (Gossypium hirsutum) 叶片蛋白质组进行了分析, 发现24个蛋白点的丰度产生了显著变化, 从而鉴定了一些盐胁迫应答蛋白。王哲等[13]用含磷和缺磷的完全营养液处理水培6 d后的甘蓝型油菜幼苗根系, 发现有62个在处理与对照之间差异显著的蛋白点。其中25个蛋白受胁迫上调表达, 37个蛋白受胁迫下调表达。王小丽等[14]对低温胁迫下玉米 (Zea mays) 叶片蛋白质组进行了研究, 得到了5种新的蛋白点, 推测其与抗寒性有关。低温胁迫下, 植株通过自身的遗传性和生理、生化等方面的反应, 导致一些代谢相关蛋白以及运输相关蛋白表达量变化, 从而诱导自身产生一些与抗逆相关的反应来抵御外界胁迫[15]。因此, 本研究应用蛋白质组学方法和技术分析低温胁迫与正常生长条件下白菜型冬油菜‘陇油7号’叶片蛋白质组差异表达的变化, 筛选和鉴定一些与低温胁迫响应相关的蛋白质, 加深对白菜型冬油菜响应低温胁迫分子机制的认识, 为进一步利用基因工程技术培育新的抗寒品种以及筛选抗寒种质资源奠定基础。
1 材料与方法 1.1 试验材料与试验设计以超强抗寒 (可耐-32 ℃, 越冬率为85%以上) 白菜型冬油菜品种‘陇油7号’[16]为供试材料。于2015年9月24日选取籽粒饱满、大小一致的油菜种子, 用10%过氧化氢处理30 min, 后用无菌水冲洗2~3次, 置于铺有两层滤纸的培养皿内进行催芽 (光照14 h, 30 ℃; 黑暗10 h, 28 ℃)。待种子露白后, 播种于装有等量育苗基质的花盆 (14 cm×13 cm) 中, 育苗基质统一距花盆口2 cm处, 共20盆, 每盆4株幼苗, 于人工培养箱中培养 (培养条件为:光照14 h, 25 ℃; 黑暗10 h, 20 ℃)。待幼苗至5叶期时, 分2组处理, 每组10盆, 一组继续在上述条件下生长, 作为对照 (CK); 另一为处理组 (T) 于人工培养箱4 ℃低温胁迫处理 (培养条件为:光照14 h, 黑暗10 h)。连续处理7 d后, 分别取对照组和处理组混合叶片各3份, 液氮速冻, 置-80 ℃贮存用于提取组织总蛋白。试验材料所需养分来自育苗基质, 其成分为蛭石、珍珠岩、草炭和有机肥, 其氮磷钾含量≥6%, 有机质≥45%。购买于甘肃省农业科学院, 材料每隔1~2 d浇水1次, 每次浇水量均为花盆最大持水量, 进行常规管理。
1.2 白菜型冬油菜叶片蛋白质差异表达分析 1.2.1 总蛋白凝胶图谱最佳pH IPG胶条的筛选为筛选‘陇油7号’叶片总蛋白凝胶图谱高丰度表达蛋白质点分离清晰可观、低丰度表达蛋白质点分辨率高且蛋白质点分布均匀的最佳pH范围的IPG胶条, 分别选用17 cm pH 3~10和17 cm pH 4~7的IPG胶条检测蛋白质凝胶图谱分离情况, 确定最佳IPG胶条pH范围。
1.2.2 白菜型冬油菜叶片总蛋白提取与蛋白质浓度测定冬油菜叶片总蛋白提取采用TCA-丙酮沉淀法[17-20]。并分别采用本研究改进后和改进前的方法。
改进后: ①取油菜叶片, 用蒸馏水冲洗干净, 滤纸擦干后, 置于经灭菌并预冷的研钵中, 加入少量PVPP后, 加入液氮充分研磨至粉末状, 将粉末转入若干个经液氮预冷的2 mL离心管中; ②每个离心管中加入-20 ℃预冷的TCA-丙酮 (含10% TCA、0.07% DTT和0.015% PMSF), 涡旋混匀, -20 ℃冰箱过夜, 次日4 ℃、20 000×g离心30 min, 弃上清留沉淀; ③每管加入约2 mL 100%冷丙酮 (含0.07% DTT和0.015% PMSF), 涡旋混匀, -20 ℃静置1 h后4 ℃、20 000 ×g离心20 min, 弃上清留沉淀, 重复此步骤1~2次, 待沉淀呈乳白状, 上清透明为宜; ④加入约2 mL 80%冷丙酮 (含0.07% DTT和0.015% PMSF), 涡旋混匀, -20 ℃静置30 min后4 ℃, 20 000 ×g离心15 min, 弃上清留沉淀, 重复此操作1~2次; ⑤将装有沉淀的离心管放入冷冻干燥机中干燥至白色粉末状后加入一定量的蛋白裂解液 (DTT现加), 室温裂解2 h, 期间每隔30 min进行涡旋混匀, 4 ℃、20 000 ×g离心30 min, 取上清即为油菜叶片总蛋白质, 定量分装, -70 ℃保存备用。
改进前:蛋白提取液中未加入PVPP、DTT和PMSF, 其余步骤同改进后方法。
1.2.3 蛋白质定量采用Bradford[20]法测定蛋白质浓度。
1.2.4 蛋白质双向电泳对低温胁迫处理和对照 (CK) 的油菜叶片总蛋白质进行双向电泳, 第1向等点聚焦 (IEF) 分别使用pH 3~10和pH 4~7的IPG胶条, 按照GE Healthcare双向电泳操作手册操作, 样品上样量为1 000 μg, 将样品与水化液按体积比1:4混匀, 总体积500 μL, 按表 1程序进行, 第2向采用浓度为12%丙烯酰胺凝胶进行SDS-PAGE电泳。电泳结束经考马斯亮蓝染色、脱色后通过UMAX的Powerlook 2100XL扫描采集图像, 用PDQuest 8.0分析软件对凝胶图谱标准化处理, 蛋白质点匹配和生物统计, 确定差异表达蛋白点。各组蛋白检测重复3次。
| 表1 等电聚焦电泳程序 Table 1 Isoelectric focusing electrophoresis procedure |
运用PDQuest 8.0分析3次重复凝胶图谱。将3张图谱在同一位置出现的差异蛋白点确定为差异蛋白点, 差异蛋白点回收、酶解[21]后送往上海中科新生命生物科技有限公司进行MALDI-TOF-TOF MS分析, 将所得到的肽片段质量数据运用PMF分析软件MASCOT 2.2进行分析, 鉴定相关的蛋白质点。所得蛋白质结果信息检索于数据库 (NCBI: http://www.ncbi.nlm.nih.gov/protein/) 和EMBL-EBL (http://www.ebi.ac.uk/services/proteins)。
1.3 数据分析利用Microsoft Excel 2010对数据处理制表和SPSS 17.0软件对数据进行显著性分析。
2 结果与分析 2.1 提取方法对油菜叶片总蛋白浓度和除盐时间的影响由表 2可以看出, 经过多次重复试验, 改进前提取方法 (未加PVPP和DTT) 得到的冬油菜叶片总蛋白浓度平均为8.11 μg·μL-1, IEF除盐时间平均为6.51 h; 改进后 (加入PVPP和DTT) 得到的全蛋白浓度平均为11.53 μg·μL-1, IEF除盐时间平均为5.37 h。由表 2可知改进后蛋白浓度及除盐时间与改进前差异达极显著水平 (P < 0.01)。因此, 通过蛋白提取液的改进, 使得叶片中蛋白质溶解更加充分, 蛋白质浓度更高, 可以更好地满足双向电泳上样量的要求; 另外, 提取液中加入PVPP, 可以有效地去除样品中酚类等杂质, 提高蛋白纯度, 减少样品中的盐分, 有利于双向电泳等电聚焦IEF过程的进行。
| 表2 冬油菜叶片总蛋白提取方法改进前后蛋白浓度和除盐时间的比较 Table 2 Protein concentrations and desalination times before and after improvement of extraction methods of protein in Brassica campestris |
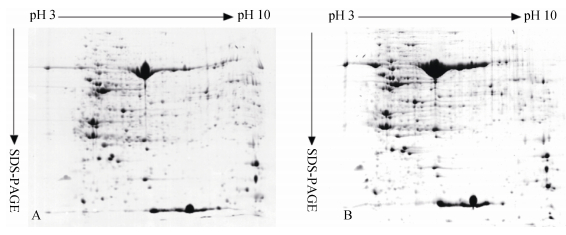
由图 1(A、B)可知, 冬油菜‘陇油7号’叶片总蛋白采用宽范围 (17 cm, pH 3~10) 非线性IPG胶条进行分离, 低温胁迫前后蛋白点主要集中在酸性 (pH 4~7) 范围内。蛋白凝胶图谱经PDQuest 8.0软件检测分析, 可以检测到800~900个蛋白点。为了让蛋白点分离更加明显清晰, 本试验又采用了窄范围 (17 cm, pH 4~7) 的IPG胶条进行蛋白点的分离 (图 2、图 3), 与宽范围 (pH 3~10) 非线性胶条相比, 窄范围 (pH 4~7) 胶条对‘陇油7号’叶片蛋白质分离效果好, 分辨率高且蛋白点分布均匀, 在凝胶图谱上可检测到600~700个蛋白点。可见, 17 cm、pH4~7线性IPG胶条更适合于油菜叶片总蛋白质的分离。
|
图 1 常温对照 (A) 和低温胁迫 (B) 下油菜叶片pH 3~10的胶条各处理叶片总蛋白双向电泳蛋白表达图谱 Figure 1 Two-dimensional electrophoresis protein expression profiles of total proteins analyzed under pH 3-10 strips of Brassica campestris leaves under normal condition (A) and cold stress of 4 ℃ for 7 days (B) |

|
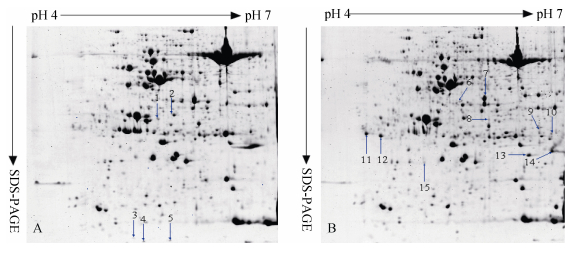
图 2 PMSF对常温处理下‘陇油7号’叶片总蛋白双向电泳蛋白表达图谱的影响 Figure 2 Effect of PMSF on the two-dimensional electrophoresis graphs of protein in seedling leaves of Brassica campestris under normal condition A:提取液不含PMSF条件下的蛋白表达图谱; B:提取液含有PMSF条件下的蛋白表达图谱。A: the two-dimensional electrophoresis protein graphs without PMSF in extraction solution; B: the two-dimensional electrophoresis protein graphs with PMSF in extraction solution. |
|
图 3 常温对照 (A) 和低温胁迫 (B) 下油菜幼苗叶片差异蛋白表达图谱 Figure 3 Two-dimensional gel electrophoresis graphs of protein in seedlings leaves of Brassica campestris under normal condition (A) and cold stress of 4 ℃ for 7 days (B) |
植物细胞破碎后, 释放的蛋白酶会降解蛋白质, 使得双向电泳凝胶图谱中的部分蛋白点缺失 (图 2A)。因此, 本试验在样品提取液中加入蛋白酶抑制剂苯甲基磺酰氟 (PMSF) 有效防止了蛋白质的降解 (图 2B)。
经PDQuest 8.0软件分析表明, 未加PMSF的凝胶图谱中可检测到的蛋白点数为587个, 而加入PMSF的凝胶图谱中可检测到的蛋白点数为661个。所以, 在样品制备过程中应尽可能的避免因蛋白质的降解而使得蛋白质种类减少, 给试验结果带来分析误差。
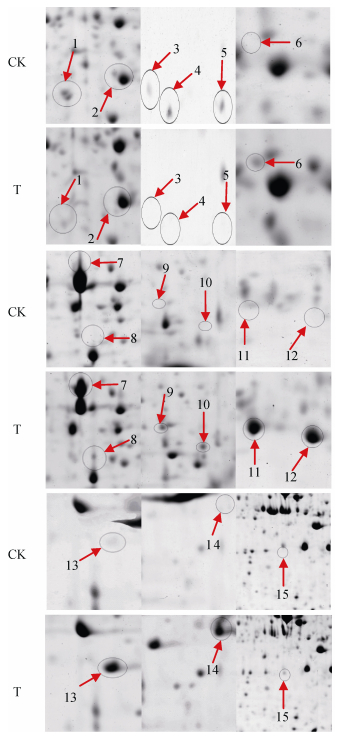
2.4 低温胁迫下油菜叶片差异蛋白点图谱分析扫描得到了蛋白质斑点清晰的低温胁迫前后油菜叶片双向电泳图谱, 且每个样品的3次电泳重复图谱基本一致。使用PDQuest 8.0软件分析2-DE的考染图 (图 3中A、B) 进行自动匹配, 并结合肉眼观察及手动调整, 检测到低温胁迫前平均蛋白点数672个, 匹配率为93%, 胁迫后平均蛋白点数689个, 匹配率为90%。对表达量变化在2倍以上的新出现的蛋白点进行检测, 共检测到‘陇油7号’叶片低温胁迫前和低温胁迫后之间有15个质变表达差异的新蛋白质点。在低温胁迫下, 植株体内原有蛋白质的含量发生明显变化, 以适应逆境胁迫, 其双向电泳凝胶图谱与对照不同, 这意味着低温胁迫影响油菜叶片可溶性蛋白质结构与组分的变化。当植物受低温胁迫刺激时, 诱导相关基因的表达, 合成一些新的蛋白质 (图 3B中6-15, 图 4), 即诱导表达的蛋白质点。这些结果表明, 在正常条件下, 某些蛋白质的表达丰度较低或不表达。但是, 在低温胁迫下, 这些蛋白质才表达、并发挥功能, 使植物体内发生一系列生理生化变化, 进而使植物耐受或抵御低温的胁迫。同时, 低温导致一些正常基因表达通路受阻, 使体内部分原有蛋白质的表达受到抑制 (图 3A中1-5, 图 4), 即抑制表达蛋白点。低温胁迫下, 相关基因的上调表达和下调表达, 是植物对不良生存环境的适应性反应。
|
图 4 低温胁迫前后‘陇油7号’幼苗叶片15个差异蛋白质点的放大图 Figure 4 Enlarged profiles of 15 differentially expressed protein spots in seedling leaves of Brassica campestris before and after low temperature stress of 4 ℃ for 7 days 椭圆区域为低温胁迫前后差异表达蛋白点。The elliptical areas denote the differentially expressed proteins before and after low temperature stress. |
对低温胁迫后15个差异蛋白点检测,成功鉴定出11蛋白点,未成功鉴定点4个,将成功鉴定的11个蛋白质谱数据与NCBI蛋白质数据库进行对比, 获取差异表达蛋白质点的相关信息 (表 3), 所鉴定得到的11个差异蛋白质分别为光合作用相关的蛋白 (蛋白点1、5、8、15)、糖代谢相关的蛋白 (蛋白点7)、物质运输相关的蛋白 (蛋白点2、6) 和胁迫响应的蛋白 (蛋白点9、10、13、14)。
| 表3 低温胁迫下‘陇油7号’幼苗叶片特异蛋白点MALDI-TOF-TOF MS质谱鉴定结果 Table 3 Identification results of special proteins of seedling leaves of Brassica campestris under cold stress of 4 ℃ for 7 days by MALDI-TOF-TOF MS |
为了完整地获取某一组织或器官在特定时期表达的蛋白种类和数量, 最大限度地避免蛋白损失和降解, 是双向电泳成败的首要环节[22]。由于白菜型冬油菜叶片中含有大量的酚类、醌类、多糖类、脂类和色素等植物次生代谢产物, 这些物质的存在会严重干扰第一向IEF[23-25]。所以, 本试验在样品提取过程中加入适量的PVPP, 有效地减少了上述物质对聚焦过程造成影响, 再通过加大离心力及延长离心时间可以除去样品中的盐分从而避免因盐分过高导致聚焦电压达不到预设电压的问题。王晋峰等[26]发现, 浓度为80%的丙酮对蛋白质沉淀效果最佳, 因此, 本试验选择用80%的冷丙酮做最后的抽提, 更加彻底地清洗了提取液中无机离子, 减少了由无机离子引起的导电性, 并达到除杂的目的。由于植物细胞内含有蛋白水解酶, 在样品研磨过程中, 细胞破碎会释放到溶液中, 引起蛋白质的水解[27]。所以本试验在蛋白提取液中加入了0.015% PMSF蛋白酶抑制剂, 有效地防止了油菜总蛋白的水解。双向电泳要求样品中的蛋白质必须完全溶解、解聚、变性和还原, 使蛋白质在第一向等电聚焦电泳中有效分离。由于β-巯基乙醇还原能力较差, 且具有特殊臭味、挥发性强, 故本试验采用还原性较强、挥发性弱的DTT替代, 以充分破坏蛋白质间的二硫键, 使蛋白更好地分离。在蛋白质组学中, 研究差异蛋白质时, 作为比对两种状态下的总蛋白在上样量上应该处于同一水平。一般情况下, 双向电泳的蛋白质上样量在0.5~1.2 mg之间。上样量过高, 一方面导致胶条对样品吸收不充分, 产生纵横条纹, 蛋白点分离效果不好; 另一方面使一些低丰度的蛋白点被高丰度蛋白点所掩盖, 难以准确地挖取目标蛋白点, 导致质谱分析的蛋白种类繁多, 鉴定结果不准确。上样量过低, 一方面不能满足考马斯亮蓝显色的要求[28]; 另一方面会造成凝胶图谱中蛋白点模糊不清, 从而导致凝胶图谱中假阳性存在, 给后续的分析工作带来困难。所以, 本试验蛋白上样量为1 mg, 获得的蛋白质斑点数清晰、没有条纹状蛋白, 得到了较好的2-DE图谱, 有利于后续的分析研究。
3.2 pH 4~7的非线性IPG胶条是白菜型冬油菜叶片总蛋白图谱分离鉴定的最佳胶条试验初期采用宽范围 (17 cm, pH 3~10) 非线性IPG胶条进行了蛋白点的预分离, 发现蛋白点主要集中在酸性 (pH 4~7) 区域内, 许多蛋白点呈簇状出现, 未能有效分离, 凝胶图谱经PDQuest 8.0软件可检测到800~900个蛋白点。但是, 目前大多数参与植物体生命活动 (如光合作用、呼吸代谢及响应逆境等) 的功能蛋白都属低丰度蛋白[29]。因而本试验选用17 cm, pH 4~7的IPG胶条进行蛋白点的分离, 可检测到600~700个蛋白点, 虽然损失了一部分蛋白点, 但是分离效果明显优于前者, 分离所得蛋白点在凝胶图谱上分布较为均匀且蛋白点清晰, 为寻找和鉴定与冬油菜抗寒功能相关的蛋白奠定了基础。
3.3 低温胁迫相关蛋白的功能分析 3.3.1 光合作用相关蛋白放氧增强蛋白 (蛋白点1) 主要功能是催化水裂解而放出氧气, 还原质体醌, 产生跨膜质子电化学势梯度。Sugihara等[30]和Yamada等[31]研究发现, 植物受到低温、干旱和盐等逆境胁迫会导致与光合作用相关蛋白发生降解, 使植物光能利用效率下降, 更容易受到光抑制。核酮糖-1, 5-二磷酸羧化酶/加氧酶 (蛋白点5) 是植物光合作用过程中的关键酶, 其活性与光合作用密切相关[32]。本研究发现该蛋白点在低温胁迫后被抑制表达, 说明低温环境下, ‘陇油7号’叶片的光合机构受损, 进行光合作用的质子传递和光合磷酸化过程受到低温抑制。光系统Ⅱ23 kD外周蛋白 (蛋白点15), 结合于类囊体膜的囊腔侧, 具有维持PSⅡ水裂解活性的功能[33]。低温胁迫后, ‘陇油7号’叶片为了维持稳定的光合速率进而诱导外周蛋白的表达来抵抗低温胁迫; 碳酸酐酶 (蛋白点8), 是细胞内催化CO2可逆水合反应的一种含锌金属水化酶, 与光合作用密切相关。邓秋红等[33]研究证明碳酸酐酶参与逆境胁迫的生物化学途径; 陈虎等[34]以龙眼 (Dimocatpus longan) 为材料, 利用差异蛋白质组学鉴定了CA蛋白, 从蛋白质水平研究表明, CA蛋白在低温胁迫下表现上调, 说明其基因与低温逆境之间存在一定关系。‘陇油7号’在低温胁迫后, 碳酸酐酶被诱导表达, 可能是植物为了适应低温胁迫需要能量来维持自身的生长。
3.3.2 糖代谢相关蛋白果糖-1, 6-二磷酸醛缩酶 (蛋白点7) 是糖酵解和糖异生过程中的一个关键酶, 该酶主要参与可溶性糖的合成及响应低温胁迫诱导表达, 可溶性糖作为渗透调节物质, 一方面可以防止细胞质内冷凝, 避免形成的冰晶对细胞造成机械损伤; 另一方面可以维持细胞内渗透压, 提高组织含水量, 降低细胞质冰点, 从而提高植物对低温的耐受性。本研究表明, 该酶属于诱导性表达蛋白质,低温胁迫后, 该蛋白迅速表达并积累, 从而保证了‘陇油7号’叶片响应低温胁迫过程中正常的糖代谢途径。汤晓丽[35]在拟南芥 (Arabidopsis thaliana) 的研究中通过表型分析及基因芯片检测发现, 在低温致死突变体中, 果糖-1, 6-二磷酸醛缩酶基因 (CpFBA) 的表达明显上调。孙得壬[36]研究发现, 在一定阈值的低温胁迫下, 都会诱导不同小麦 (Triticum aestivum) 品种CpFBA的表达响应, 表达量显著上调, 从而使相应蛋白质合成并不断积累, 这与本研究结果相类似。
3.3.3 物质运输相关蛋白转录调控锌指蛋白 (蛋白点2) 是一种转录调控因子。它可以通过特定的结构域与抗寒靶基因启动子区域的顺式调控元件特异结合来应答外界环境胁迫[37]。此类蛋白的表达可使植物更有效地应对低温胁迫。目前从棉花、矮牵牛 (Petunia hybrid) 等植物中获得的该类基因一般都参与植物生长发育与抗逆反应[38-39]。但是, 在本研究中该蛋白在低温胁迫后被抑制表达, 说明‘陇油7号’叶片在长时间低温胁迫后, 叶片组织蛋白的结构域受到破坏, 致使抗寒靶基因未能与蛋白结构域特异结合。膜联蛋白 (蛋白点6) 是一类Ca2+及磷脂结合蛋白, 植物细胞中annexin的研究起步较晚。目前, 已发现annexin蛋白在植物体广泛分布, 在植物生长发育和应对环境胁迫过程中起重要作用, 主要参与了抗寒反应、细胞分泌、Ca2+代谢、耐盐胁迫、干旱胁迫以及ABA信号转导[39]。何美敬等[40]研究发现膜联蛋白在细胞内具有过氧化物酶活性, 可以推测该蛋白点的诱导表达。可见转录调控锌指蛋白对于清除低温胁迫下‘陇油7号’叶片中积累的活性氧, 以此保证逆境胁迫下物质的正常运输具有重要作用。
3.3.4 逆境响应相关蛋白巯基蛋白酶抑制剂 (蛋白点9、10) 具有保护细胞、组织及器官中蛋白质免遭外源蛋白水解酶水解的作用[41]。此外, 研究表明, 蛋白水解酶抑制剂基因的超表达也能提高转基因植物抗低温、干旱等非生物胁迫能力。沙冬青 (Ammopiptanthus mongolicus) 是我国西北重要的抗逆植物资源, Liu等[42]克隆到了沙冬青低温诱导Amp I基因, 经鉴定属于巯基蛋白酶抑制剂基因。类甜蛋白 (蛋白点13) 是一种具有多种生物学活性及重要功能的植物防御蛋白, 植物受到生物或非生物胁迫时, 类甜蛋白在植物组织中迅速表达并积累, 从而快速提高植物抗性[43]。Hiilovaara等[44]研究发现, 冬黑麦 (Secale cereale) 叶片质外体在低温诱导下分泌的类甜蛋白, 其抗冻活性与抗冻蛋白相同。抗病毒蛋白 (蛋白点14), 一方面能够诱导植物病程相关蛋白的表达, 此蛋白在低温胁迫下不断积累进而诱导植株获得抗寒性[45]; 另一方面能够诱导其他蛋白或物质的产生, 使植株产生系统抗性, 从而抵御外界胁迫对植株造成的伤害[46]。本研究中, 低温下‘陇油7号’抗寒响应相关蛋白的表达与积累, 可有效防止低温对细胞生理、结构的损伤, 从而大大提高其抗寒能力。
4 结论17 cm、pH 4~7的IPG胶条最适于油菜叶片的蛋白点的分离。低温胁迫后, 超强抗寒白菜型冬油菜品种‘陇油7号’叶片部分光合作用相关蛋白表达受抑制, 同时又诱导部分光合作用相关蛋白的表达, 抑制表达的蛋白可能是在长时间低温条件下植物组织受到不可逆转的损伤所致。同时, 植物为了维持正常的光合作用, 诱导碳酸酐酶等光合作用关键酶的表达, 维持植株的正常生长; 膜联蛋白等物质运输相关蛋白的表达, 有助于维持细胞结构, 促进离子的跨膜运输, 维持植株体内的稳态平衡; 此外, 低温诱导产生的类甜蛋白, 与其他逆境响应蛋白协同发挥作用来抵御低温的胁迫。由可以推测, 稳定的光合作用、高效的物质代谢系统以及强大的抗逆防御机制对低温条件下维持超强抗寒品种‘陇油7号’的生长起重要的作用。
| [1] |
张学贤. 白菜型冬油菜的抗寒性分析及抗寒性相关的分子标记[D]. 杨凌: 西北农林科技大学, 2014
Zhang X X. Analysis of cold resistance and molecular markers related to cold resistance of Winter Brassica rapa[D]. Yangling:Northwest A&F University, 2014 |
| [2] |
孙万仓, 马卫国, 雷建明, 等.
冬油菜在西北旱寒区的适应性和北移的可行性研究[J]. 中国农业科学, 2007, 40(12): 2716–2726.
Sun W C, Ma W G, Lei J M, et al. Study on adaptation and introduction possibility of winter rapeseed to dry and cold areas in Northwest China[J]. Scientia Agricultura Sinica, 2007, 40(12): 2716–2726. |
| [3] |
刘自刚, 孙万仓, 杨宁宁, 等.
冬前低温胁迫下白菜型冬油菜抗寒性的形态及生理特征[J]. 中国农业科学, 2013, 46(22): 4679–4687.
Liu Z G, Sun W C, Yang N N, et al. Morphology and physiological characteristics of cultivars with different levels of cold-resistance in winter rapeseed (Brassica campestris L.) during cold acclimation[J]. Scientia Agricultura Sinica, 2013, 46(22): 4679–4687. |
| [4] |
贾凌云, 张腾国, 于娟, 等.
陇油6号油菜BnMPK6基因启动子分离及序列分析[J]. 西北师范大学学报:自然科学版, 2012, 48(2): 86–90.
Jia L Y, Zhang T G, Yu J, et al. Isolation and sequence analysis of BnMPK6 gene promoter from Brassica napus (rape) longyou 6[J]. Journal of Northwest Normal University:Natural Science, 2012, 48(2): 86–90. |
| [5] |
曾秀存, 孙万仓, 方彦, 等.
白菜型冬油菜抗坏血酸过氧化物酶 (APX) 基因的克隆、表达及其活性分析[J]. 作物学报, 2013, 39(8): 400–1408.
Zeng X C, Sun W C, Fang Y, et al. Cloning, expression, and activity analysis of Ascorbate Peroxidase (APX) gene from winter turnip rape (Brassica campestris L.)[J]. Acta Agronomica Sinica, 2013, 39(8): 400–1408. |
| [6] |
曾秀存, 刘自刚, 史鹏辉, 等.
白菜型冬油菜铜锌超氧化物歧化酶 (Cu/Zn-SOD) 基因的克隆及其在低温条件下的表达[J]. 作物学报, 2014, 40(4): 636–643.
Zeng X C, Liu Z G, Shi P H, et al. Cloning and expression analysis of copper and zinc superoxide dismutase (Cu/Zn-SOD) gene from Brassica campestris L.[J]. Acta Agronomica Sinica, 2014, 40(4): 636–643. DOI:10.3724/SP.J.1006.2014.00636 |
| [7] |
蒲媛媛. 白菜型冬油菜抗寒性的生理特性与蛋白质组的电泳分析[D]. 兰州: 甘肃农业大学, 2010
Pu Y Y. Physiological characteristics evaluation and proteonmic analysis by electrophoresis and cold stress in winter rapa[D]. Lanzhou:Gansu agricultural University, 2010 |
| [8] |
解伟, 陈社员, 张振乾.
油菜蛋白质组学研究进展[J]. 中国农学通报, 2013, 29(27): 7–12.
Xie W, Chen S Y, Zhang Z Q. The advances on the proteomics of rape[J]. Chinese Agricultural Science Bulletin, 2013, 29(27): 7–12. |
| [9] |
朱宏, 王继华, 王同昌.
小麦T型细胞质雄性不育系与可育系叶片蛋白质双向电泳分析[J]. 植物研究, 2004, 24(3): 339–342.
Zhu H, Wang J H, Wang T C. Analysis of leaf proteins of T-cytoplasmic male sterility and fertility restoration in common wheat by 2D-PAGE[J]. Bulletin of Botanical Research, 2004, 24(3): 339–342. |
| [10] | Honore B. Genome-and proteome-based technologies:Status and applications in the postgenomic era[J]. Expert Review of Molecular Diagnostics, 2001, 1(3): 265–274. DOI:10.1586/erm.2001.1.issue-3 |
| [11] | Swatton J E, Prabakaran S, Karp N A, et al. Protein profiling of human postmortem brain using 2-dimensional fluorescence difference gel electrophoresis (2-D DIGE)[J]. Molecular Psychiatry, 2004, 9(2): 128–143. DOI:10.1038/sj.mp.4001475 |
| [12] |
崔宇鹏, 樊保香, 王德龙, 等.
盐胁迫下棉花叶片差异蛋白表达的分析[J]. 分子植物育种, 2012, 10(1): 48–54.
Cui Y P, Fan B C, Wang D L, et al. Analysis of differential proteins of cotton leaves under salt stress[J]. Molecular Plant Breeding, 2012, 10(1): 48–54. |
| [13] |
王哲, 余永芳, 梁从敏, 等.
低磷胁迫下甘蓝型油菜幼苗根系差异蛋白双向电泳图谱分析[J]. 西北农业学报, 2013, 22(10): 50–53.
Wang Z, Yu Y F, Liang C M, et al. Two-dimensional gel electrophoresis analysis of differential proteins of Brassica napus roots under phosphorous deficiency[J]. Acta Agriculturae Boreali-Occidentalis Sinica, 2013, 22(10): 50–53. |
| [14] |
王小丽, 裴玉贺, 张恩盈, 等.
低温胁迫下玉米叶片蛋白质的双向电泳分析[J]. 玉米科学, 2009, 17(1): 96–98.
Wang X L, Pei Y H, Zhang E Y, et al. Analysis of maize protein under cold treatment by Two-dimensional electrophoresis[J]. Journal of Maize Sciences, 2009, 17(1): 96–98. |
| [15] |
孙万仓.
北方旱寒区冬油菜栽培技术[M]. 北京: 中国农业出版社, 2013.
Sun W C. Cultivation Technology of Winter Rapeseed in Dry and Cold Areas in the North China[M]. Beijing: China Agriculture Press, 2013. |
| [16] | Meza-Basso L, Alberdi M, Raynal M, et al. Changes in protein synthesis in rapeseed (Brassica napus) seedlings during a low temperature treatment[J]. Plant Physiology, 1986, 82(3): 733–738. DOI:10.1104/pp.82.3.733 |
| [17] |
黄甫海燕, 官春云.
甘蓝型油菜抗菌核病近等基因系和感病亲本蛋白差异的初步研究[J]. 中国农业科学, 2010, 43(10): 2000–2007.
Huangfu H Y, Guan C Y. A preliminary analysis of differential proteins between Brassica napus resistance to Sclerotinia sclerotiorum near-isogenic lines and susceptible parent[J]. Scientia Agricultura Sinica, 2010, 43(10): 2000–2007. |
| [18] |
甘露, 李殿荣, 臧新, 等.
甘蓝型油菜蛋白质双向电泳体系的建立[J]. 作物学报, 2010, 36(4): 612–619.
Gan L, Li D R, Zang X, et al. Construction of protein two-dimensional polyacrylamide gel electrophoresis system for Brassica napus[J]. Acta Agronomica Sinica, 2010, 36(4): 612–619. |
| [19] |
刘海衡, 胡胜武, 刘胜毅, 等.
油菜不同器官高质量总蛋白提取方法和双向电泳体系的优化[J]. 中国油料作物学报, 2009, 31(4): 426–433.
Liu H H, Hu S W, Liu S Y, et al. Optimization of high quality total protein extraction and two-dimensional gel electrophoresis system for different Brassica napus organ[J]. Chinese Journal of Oil Crop Sciences, 2009, 31(4): 426–433. |
| [20] | Bradford M M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding[J]. Analytical Biochemistry, 1976, 72(1/2): 248–254. |
| [21] | Katayama H, Nagasu T, Oda Y. Improvement of in-gel digestion protocol for peptide mass fingerprinting by matrix-assisted laser desorption/ionization time-of-flight mass spectrometry[J]. Rapid Communications in Mass Spectrometry, 2001, 15(16): 1416–1421. DOI:10.1002/(ISSN)1097-0231 |
| [22] |
孟慧, 段翠芳, 增日中.
植物蛋白质组学研究概况[J]. 热带农业科学, 2006, 26(2): 60–64.
Meng H, Duan C F, Zeng R Z. Researches of plant proteomics[J]. Chinese Journal of Tropical Agriculture, 2006, 26(2): 60–64. |
| [23] |
范冬梅, 杨铭.
双向凝胶电泳-蛋白质组分析的核心技术[J]. 中国生化药物杂志, 2005, 26(3): 182–184.
Fan D M, Yang M. Two-dimensional electrophoresis-The key technique of proteome analysis[J]. Chinese Journal of Biochemical Pharmaceutics, 2005, 26(3): 182–184. |
| [24] |
舒佳宾, 文李, 官春云.
甘蓝型油菜叶片蛋白质双向电泳体系优化[J]. 作物研究, 2012, 26(4): 350–354.
Shu J B, Wen L, Guan C Y. Optimization of two dimensional polyacrylamide gel electrophoresis system for Brassica napus leaves protein[J]. Crop Research, 2012, 26(4): 350–354. |
| [25] |
王玉琪, 彭新湘.
适用于水稻叶片蛋白质组分析的双向电泳技术[J]. 植物生理与分子生物学学报, 2006, 32(2): 252–256.
Wang Y Q, Peng X X. A two-dimensional electrophoresis protocol suitable for proteomic study of rice leaves[J]. Journal of Plant Physiology and Molecular Biology, 2006, 32(2): 252–256. |
| [26] |
王晋峰, 刘凌, 郑玉才, 等.
植物叶蛋白提取技术及开发利用研究[J]. 草业科学, 2003, 20(1): 7–11.
Wang J F, Liu L, Zheng Y C, et al. Technology for plant leaf protein extraction and utilization[J]. Pratacultural Science, 2003, 20(1): 7–11. |
| [27] |
汪家政, 范明.
蛋白质技术手册[M]. 北京: 科学出版社, 2000: 11-48.
Wang J Z, Fan M. The Technical Manuals of Protein[M]. Beijing: Science Press, 2000: 11-48. |
| [28] |
李新华, 张万岱, 王波涛, 等.
胃粘膜组织蛋白质组双向凝胶电泳技术的初步建立与优化[J]. 解放军医学杂志, 2003, 28(5): 438–440.
Li X H, Zhang W D, Wang B T, et al. Preliminary establishment and optimization of two-dimensional gel electrophoresis for proteomics of gastric mucosa[J]. Medical Journal of Chinese People's Liberation Army, 2003, 28(5): 438–440. |
| [29] | Donnelly B E, Madden R D, Ayoubi P, et al. The wheat (Triticum aestivum L.) leaf proteome[J]. Proteomics, 2005, 5(6): 1624–1633. DOI:10.1002/(ISSN)1615-9861 |
| [30] | Sugihara K, Hanagata N, Dubinsky N, et al. Molecular characterization of cDNA encoding oxygen evolving enhancer protein 1 increased by salt treatment in the mangrove Bruguiera gymnorrhiza[J]. Plant & Cell Physiology, 2000, 41(11): 1279–1285. |
| [31] | Yamada K, Lim J, Dale J M, et al. Empirical analysis of transcriptional activity in the Arabidopsis genome[J]. Science, 2003, 302(5646): 842–846. DOI:10.1126/science.1088305 |
| [32] |
陈为钧, 赵贵文, 顾月华.
RubisCO的研究进展[J]. 生物化学与生物物理进展, 1999, 26(5): 433–436.
Chen W J, Zhao G W, Gu Y H. Advance of ribulose-1, 5-bisphosphate carboxylase/oxygenase (RubisCO)[J]. Progress in Biochemistry and Biophysics, 1999, 26(5): 433–436. |
| [33] |
邓秋红, 甘露, 付春华, 等.
芸薹属中几个物种碳酸酐酶活性的比较[J]. 植物生理学通讯, 2009, 45(7): 663–666.
Deng Q H, Gan L, Fu C H, et al. Comparison of carbonic anhydrase activities of several species in Brassica[J]. Plant Physiology Communications, 2009, 45(7): 663–666. |
| [34] |
陈虎, 何新华, 罗聪, 等.
低温胁迫下龙眼碳酸酐酶基因 (CA) 的克隆与表达分析[J]. 园艺学报, 2012, 39(2): 243–252.
Chen H, He X H, Luo C, et al. Cloning and expression of longan carbonic anhydrase gene under low temperature stress[J]. Acta Horticulturae Sinica, 2012, 39(2): 243–252. |
| [35] |
汤晓丽. 拟南芥两个胞质果糖-1, 6-二磷酸醛缩酶基因的新功能初探[D]. 泰安: 山东农业大学, 2013
Tang X L. New functional studies of two cytosolic fructose bisphosphate aldolase genes in Arabidopsis[D]. Taian:Shandong Agricultural University, 2013 |
| [36] |
孙得壬. 小麦叶绿体果糖-1, 6-二磷酸醛缩酶在非生物胁迫中的表达及其遗传转化研究[D]. 杨凌: 西北农林科技大学, 2013
Sun D R. Study on the genetic transformation and expression of wheat chloroplast fructose-1, 6-bisphosphate aldolase gene in abiotic stress[D]. Yangling:Northwest A & F University, 2013 |
| [37] | Gaiser J C, Robinson-Beers K, Gasser C S. The Arabidopsis SUPERMAN gene mediates asymmetric growth of the outer integument of ovules[J]. The Plant Cell, 1995, 7(3): 333–345. DOI:10.1105/tpc.7.3.333 |
| [38] |
杨郁文, 周建武, 张保龙, 等.
棉花SUPERMAN类锌指蛋白基因GZFP的启动子及功能分析[J]. 棉花学报, 2011, 23(6): 483–489.
Yang Y W, Zhou J W, Zhang B L, et al. Functional analysis of the SUPERMAN-like zinc finger protein gene GZFP and its promoter[J]. Cotton Science, 2011, 23(6): 483–489. |
| [39] |
张娜, 尚忠林.
植物细胞中的膜联蛋白 (annexin)[J]. 植物生理学通讯, 2010, 46(3): 277–283.
Zhang N, Shang Z L. Annexins in plant cells[J]. Plant Physiology Communications, 2010, 46(3): 277–283. |
| [40] |
何美敬, 穆国俊, 侯名语, 等.
植物膜联蛋白的结构及功能研究进展[J]. 西北植物学报, 2013, 33(12): 2567–2574.
He M J, Mu G J, Hou M Y, et al. Advances in structure and function of plant Annexins[J]. Acta Botanica Boreali-Occidentalia Sinica, 2013, 33(12): 2567–2574. |
| [41] |
刘瑞玲, 刘美芹, 史军娜, 等.
过量表达沙冬青巯基蛋白酶抑制剂基因AmPI提高大肠杆菌低温与热胁迫抗性[J]. 应用与环境生物学报, 2010, 16(3): 341–346.
Liu R L, Liu M Q, Shi J N, et al. Heterologous expression of Ammopiptanthus mongolicus cysteine proteinase inhibitor gene AmPI enhances Escherichia coli viability under cold and heat stresses[J]. Chinese Journal of Applied & Environmental Biology, 2010, 16(3): 341–346. |
| [42] | Liu M Q, Shen X, Yin W L, et al. Functional analysis of cold-inducible cDNA clones in the Legume Ammopiptanthus mongolicus[J]. Cryoletters, 2005, 26(4): 213–222. |
| [43] |
李文娴, 刘迪秋, 丁元明, 等.
类甜蛋白的结构特征以及功能研究进展[J]. 中国生物工程杂志, 2010, 30(3): 100–104.
Li W X, Liu D Q, Ding Y M, et al. Research progress in the structural features and functions of thaumatin-like proteins[J]. China Biotechnology, 2010, 30(3): 100–104. |
| [44] | Hiilovaara-Teijo M, Hannukkala A, Griffith M, et al. Snow-mold-induced apoplastic proteins in winter rye leaves lack antifreeze activity[J]. Plant Physiology, 1999, 121(2): 665–674. DOI:10.1104/pp.121.2.665 |
| [45] |
陆许可, 张德超, 阴祖军, 等.
干旱胁迫下不同抗旱水平陆地棉的叶片蛋白质组学比较研究[J]. 西北植物学报, 2013, 33(12): 2401–2409.
Lu X K, Zhang D C, Ying Z J, et al. Comparative analysis of proteomics in cotton (Gossypium hirsutum L.) leaves with different drought resistance levels under drought stress[J]. Acta Botanica Boreali-Occidentalia Sinica, 2013, 33(12): 2401–2409. |
| [46] | Verma H N, Awasthi L P, Saxena K C. Isolation of the virus inhibitor from the root extract of Boerhaavia diffusa inducing systemic resistance in plants[J]. Canadian Journal of Botany, 1979, 57(11): 1214–1217. DOI:10.1139/b79-146 |
 2017, Vol. 25
2017, Vol. 25



