昆虫病原线虫(entomopathogenic nematodes, EPN)是指体内携带具病原性的共生细菌, 能使节肢动物类发病并死亡的一类线虫[1-2]。该类线虫具有寄主范围广、毒力高、能主动寻找寄主、对人畜及环境安全无毒、并能人工大量培养等诸多优点, 因此作为一种有效的生防因子, 被广泛应用于地下害虫和隐蔽性害虫的防治, 具有巨大的开发潜力和应用前景[3-7]。
昆虫病原线虫营自由生活阶段, 要面临各种非生物胁迫, 包括高温、低湿、紫外辐射(UV-B)、化学感应、土壤类型等; 在实际应用中, 决定昆虫病原线虫对害虫防治效果高低的关键因子之一, 是在各种非生物因子的胁迫下, 昆虫病原线虫能否在田间建立种群。因此研究非生物胁迫对昆虫病原线虫的影响, 具有重要意义[8-10]。目前昆虫病原线虫对隐蔽性害虫的防治应用比较广泛, 其对叶面害虫的防治室内试验表明也有较好的控制效能, 但在田间应用时防治效果会有所降低, 重要的影响因子就是UV-B辐射[11]。
近年来, 随着生产和生活中大量生产和使用氯氟烃等消耗臭氧层的物质, 以及大量废气的排放, 破坏大气臭氧层, 并导致地面紫外辐射(UV-B)增加。过量紫外线对人类、动植物、微生物等会产生危害, 并产生明显的生物学效应[11-15]。研究表明, 紫外线辐射对秀丽隐杆线虫(Caenorhabditis elegans)具有一定的影响, 主要表现在生殖毒性, 但是研究同时表明适当的紫外辐射预处理可防止行为缺陷机制的形成[15]。有关紫外辐射对昆虫病原线虫的影响和昆虫病原线虫对紫外辐射的抗逆性和适应性, 相关报道较少[9]。本项目组前期研究发现甘肃省昆虫病原线虫资源丰富, 分布广泛且对甘肃省主要的地下害虫有较高的控制作用, 说明本土昆虫病原线虫对低湿、高温和紫外辐射等逆境有一定的耐受能力[9, 16-19]。但当前环境中的UV-B辐射是否已经对昆虫病原线虫的生长发育具有一定程度的胁迫作用?甘肃省土著昆虫病原线虫, 尤其是优势种对UV-B辐射的适应性如何?尚缺少足够的了解。本研究以甘肃省土著昆虫病原线虫为材料, 通过模拟自然界强辐射的研究手段, 以昆虫病原线虫研究中常用测试昆虫大蜡螟为目标昆虫, 探究紫外辐射对昆虫病原线虫生物学特性如存活率与致病力的影响, 可为利用昆虫病原线虫防治叶面害虫提供理论依据, 以期进一步揭示昆虫病原线虫对UV-B辐射的适应特性。
1 材料与方法 1.1 供试材料大蜡螟(Galleria mellonella)由甘肃农业大学昆虫生态实验室养殖, 试验用5龄老熟幼虫其平均重量为0.3 g左右, 使用前需经滞育处理, 防止大蜡螟老熟幼虫吐丝、化蛹。
昆虫病原线虫:从甘肃省诱集分离得到的9个品系, 分别为异小杆属的Heterorhabditis brevicaudis的0627M品系、大异小杆线虫(H. megidis)的0641TY品系和斯氏属的Steinernema feltiae的0622L、0639C、0661YM、0619HT、0663TD品系与S. kraussei的0663HT、0657L品系。已证实上述9个昆虫病原线虫品系对低湿胁迫具较强抗逆性, 对主要地下害虫蛴螬(Scaabaeidae)和韭蛆(Bradysia difformis)具较高控制效能[9, 16-17]。均由大蜡螟老熟幼虫White trap法培养, 试验用的感染期线虫均新鲜培养, 并用0.2%柳硫汞进行表面消毒, 贮存于4 ℃备用。
1.2 紫外(UV-B)辐射对昆虫病原线虫存活率影响的测定本试验于24孔板中进行。将加有9个线虫品系悬浮液的24孔板, 每孔加入线虫悬浮液1 000 μL(含线虫1 000头), 每品系3孔, 暴露于20 W和40 W紫外辐射灯下20 cm处(60 μW·cm–2、100 μW·cm–2)分别处理0.5 h、1 h、1.5 h、2 h、3 h、4 h、5 h和6 h。以未经紫外辐射的9个线虫品系悬浮液为对照。到达处理时间后取出, 在室温下放置1 h, 使线虫充分复苏, 复苏后统计每个处理中昆虫病原线虫的活虫平均数及平均存活率。
| $ 线虫存活率\left( \% \right) = \frac{存活线虫数}{总线虫数} \times 100 $ | (1) |
采用改良的ONE ON ONE法测定[1, 17]。于24孔板中, 每孔放2 g经灭菌的细沙, 加无菌水使含水量为15%(w/w), 每孔放1头大蜡螟5龄幼虫, 滴入经20 W紫外辐射30 min的线虫悬浮液50 mL[每孔50头侵染期线虫(IJs)]。不同的线虫品系为不同处理, 以未经紫外辐射的线虫做相应对照组, 每处理重复15次(15孔), 置于(25±1) ℃白天/(18±1) ℃夜晚、8 h白天/16 h夜晚, 相对湿度80%的恒温箱内。每隔8 h观察记录大蜡螟死亡情况。
1.3.2 紫外(UV-B)辐射强度及时长对Steinernema feltiae 0639C和0663TD致病力影响的测定于24孔板中, 每孔放2 g经灭菌的细沙, 加无菌水使含水量为15%(w/w), 每孔放1头大蜡螟5龄幼虫, 滴入经20 W和40 W的UV-B辐射强度处理30 min、60 min、90 min、120 min的S. felitiae 0639C和0663TD的悬浮液50 L(50 IJs·孔–1), 以未经紫外辐射的线虫做相应对照组。每处理重复10次, 置于(25±1) ℃白天/ (18±1)℃夜晚、8 h白天/16 h夜晚, 相对湿度80%的恒温箱内。每隔8 h观察记录大蜡螟死亡情况, 比较各处理强度UV-B辐射下昆虫病原线虫对大蜡螟致病力的影响。
试验数据用SPSS 21.0和Microsoft Excel 2016进行统计分析。
2 结果与分析 2.1 UV-B辐射对昆虫病原线虫存活率的影响表 1表明, 经20 W和40 W紫外灯辐射0.5 h后, 昆虫病原线虫H. brevicaudis 0627M、H. megidis 0641TY、S. feltiae 0622L、S. feltiae 0639C、S. feltiae 0661YM、S. feltiae 0619HT、S. feltiae 0663TD、S. kraussei 0663HT、S. kraussei 0657L 9个品系(除S. feltiae 0622L 40 W外)与未辐射处理存活率差异不显著(P > 0.05), 且不同品系之间差异不显著(P > 0.05), 说明以上9个品系昆虫病原线虫均对短时间UV-B辐射有一定的耐受力。
| 表 1 不同时间不同强度UV-B辐射对不同昆虫病原线虫品系存活率的影响 Table 1 Entomopathogenic nematodes infective juveniles (IJs) survival rate at different ultraviolet radiation intensities under different exposure time length |
20 W、40 W紫外辐射灯处理下, 辐射时长对昆虫病原线虫存活率有显著影响。随着辐射时长的延长, 供试的9个昆虫病原线虫的存活率均逐步降低, 且在辐射时长大于2 h后, 存活率急剧下降, 与未经辐射的对照组相比较差异显著(P < 0.05)。辐射时长为6 h时, 供试各品系存活率均在10%以下, 但各品系之间差异不显著(P > 0.05), 其中S. feltiae 0639C、0661YM、S. kraussei 0663HT存活率为0。当辐射强度为20 W时, 2 h的辐射时长为对昆虫病原线虫存活率影响较大的时间节点, 时长为2 h以内时, 除S. feltiae 06622L和S. kraussei 0663HT 2品系外, 不同辐射时长下, 其余供试7个昆虫病原线虫品系的存活率无显著变化, 与对照组之间差异不显著(P > 0.05), 不同品系之间除S. kraussei 0663HT与其他供试8品系差异显著(P < 0.05)外, 其余各品系之间差异不显著(P > 0.05);但时长大于2 h后, 供试的9个昆虫病原线虫品系存活率均急剧下降, 因此后期研究均以2 h作为辐射时长的上限。辐射强度为40 W时, 辐射时长为0.5 h时, 除S. feltiae 0622L品系存活率与对照组差异显著(P < 0.05), 其余供试品系与对照组差异均不显著(P > 0.05), 且各品系之间差异不显著(P > 0.05);其余各辐射时长下, 供试9个昆虫病原线虫品系均随着辐射时长的增加, 其存活率下降且与对照组差异显著(P < 0.05)。说明随着UV-B辐射时间的延长, 昆虫病原线虫对UV-B辐射的抵抗力降低。长时间UV-B辐射对不同昆虫病原线虫品系存活率的影响不同。经UV-B辐射4 h内, H. megidis 0627M的存活率较高, 说明H. megidis 0627M对长时间UV-B辐射有一定的耐受能力。
不同辐射强度对昆虫病原线虫存活率影响不同, 辐射时长在2 h之内, 随着辐射强度的增加, 昆虫病原线虫存活率降低, 40 W与20 W差异显著(P < 0.05), 2 h之后不同辐射强度之间差异不显著(P > 0.05)。同一辐射强度时, 线虫存活率随着辐射时长的增加下降, 但在2 h之内, 各辐射时长之间线虫存活率无显著差异(P > 0.05), 2 h之后各品系线虫存活率均显著降低, 与对照组差异显著(P < 0.05)。综上所述, 辐射时长在2 h内, UV-B强度是影响昆虫病原线虫存活率的主要因子, 辐射时长对其存活率无显著影响。
2.2 UV-B辐射对不同昆虫病原线虫种类和品系致病力的影响表 2表明, 20 W UV-B辐射30 min后, 昆虫病原线虫对大蜡螟的致病力发生变化, 不同种类和同一种类的不同品系变化不同。供试的9个品系中, S. felitiae 0663TD致病力升高, 而S. felitiae 0661YM降低。其中S. felitiae 0639C在侵染后32 h和40 h时差异显著(P < 0.05), 分别由13.3%和20.0%升高到73.3%和86.6%; S. felitiae 0661YM在侵染32 h、40 h时, 经UV-B辐射的处理死亡率均为0%, 而未经辐射处理的均达66.7%, 差异显著(P < 0.05);而其余各品系致病力未改变或下降, 且各品系之间差异不显著(P > 0.05)。
| 表 2 20W UV-B辐射30 min下不同昆虫病原线虫品系对大蜡螟致病力的影响 Table 2 Effects of 20 W ultraviolet radiation after 30 min exposure on entomopathogenic nematodes' pathogenicity to Galleria mellonella |
UV-B辐射使异小杆属H. megidis 0641TY和H. brevicaudis 0627M 2个品系致病力下降, 且使寄主死亡的时间推后(表 2)。经UV-B辐射30 min后, H. megidis 0641TY和H. brevicaudis 0627M致病力均下降, 但无显著差异(P > 0.05);值得注意的是, 2线虫品系对大蜡螟的致死速率均有延后。接入H. brevicaudis 0627M 72 h时, 对照组大蜡螟累积死亡率为80.0%, 处理组为73.3%; 80 h时对照组死亡率达100%, 而处理组在88 h后才达100%; H. megidis 0641TY对照组和处理组在32 h时引起大蜡螟死亡; 接入线虫112 h后, 对照组死亡率达100%, 而处理组在接入线虫120 h后大蜡螟死亡率达100%。说明UV-B辐射降低异小杆属线虫的致病力, 并延缓引起寄主昆虫死亡的时间。
2.2.2 UV-B处理后斯氏属线虫对大蜡螟致病力的影响经UV-B处理后斯氏属线虫对大蜡螟的致病力也发生变化, 但不同种类、同一种类不同品系之间均存在差异。S. felitiae 5个供试品系, 0639C、0663TD 2品系经UV-B辐射后对大蜡螟的致病力提高, 致死速率加快, 其中S. felitiae 0663TD的致病力显著升高(P < 0.05); S. felitiae 0622L品系经UV-B辐射后其致病力无显著变化(P > 0.05), 且死亡速率基本相同(表 2); S. felitiae的0661YM和0619HT经UV-B辐射后, 其致病力均呈降低趋势, 其中S. felitiae 0661YM的致病力显著降低(P < 0.05), 其余差异不显著(P > 0.05); S. kraussei 0657L和0663HT品系经UV-B辐射后, 致病力均下降, 但差异均不显著(P > 0.05)。
2.2.2.1 S. felitiae 0639C和0663TD供试品系经UV-B辐射30 min后, S. felitiae 0639C和0663TD引起全部寄主死亡时间缩短(表 2)。S. felitiae 0639C对照组和处理组均在32 h时大蜡螟开始死亡, 处理组大蜡螟累积死亡率为73.3%, 对照组为13.3%, 存在显著差异(P < 0.05);经UV-B辐射处理后, 接入线虫56 h后大蜡螟死亡率达100%, 而对照组64 h时达100%; S. felitiae 0663TD对照组在接入线虫24 h时大蜡螟开始死亡, 处理组32 h时开始死亡; 对照组在接入线虫80 h后大蜡螟死亡率为100%, 处理组在接入线虫40 h后大蜡螟的死亡率达100%。
2.2.2.2 S. felitiae 0622L供试品系S. felitiae 0622L品系经UV-B辐射后其致病力无显著变化(P > 0.05), 且死亡速率基本相同(表 2)。接入线虫32 h后, 对照组和处理组大蜡螟均开始死亡, 56 h时大蜡螟的死亡率均为73.3%;对照组112 h后死亡率达到100%, 处理组则在104 h后达100%。
2.2.2.3 S. felitiae 0661YM和0619HT品系与S. kraussei 0663HT和0657L品系经UV-B辐射后S. felitiae 0661YM和0619HT品系与S. kraussei 0663HT和0657L品系的致病力均下降, 除S. felitiae 0661YM与对照组差异显著外, 其余品系差异不显著(P > 0.05), 且寄主开始死亡时间和引起供试全部种群死亡的时间均延长(表 2)。S. felitiae 0661YM品系, 对照组侵染后32 h寄主昆虫开始死亡, 56 h时全部死亡, 而经紫外辐射后, 48 h时寄主昆虫开始死亡, 120 h时全部死亡; S. felitiae 0619HT品系, 处理组和对照组均在32 h时引起寄主昆虫死亡, 对照组56 h时寄主昆虫死亡率达100%, 而处理组在120 h时寄主昆虫死亡率达100%。
S. kraussei 0663HT品系的对照组和处理组, 均在接入线虫后32 h时大蜡螟开始死亡; 80 h时对照组大蜡螟的死亡率是86.7%, 处理组为80.0%;对照组88 h大蜡螟校正死亡率达100%, 处理组104 h时才达100%; S. kraussei 0657L品系的CK和UV-B辐射组均在接入线虫后40 h时大蜡螟开始死亡; 80 h时CK大蜡螟累积死亡率为93.3%, 处理组为73.3%; CK组88 h大蜡螟死亡率达100%, 处理组96 h时才达到100%。
综上所述, 在20W UV-B辐射30 min后, 斯氏S. felitiae 0639C的致病力显著升高(P < 0.05), S. felitiae 0661YM的致病力显著降低(P < 0.05), S. felitiae 0663TD、0622L大蜡螟的致病力升高, 异小杆H. megidis 0641TY和H. brevicaudis 0627M, 斯氏S. kraussei 0657L、0663HT和S. felitiae 0619HT、0661YM致病力下降, 但差异均不显著(P > 0.05)。说明UV-B辐射对昆虫病原线虫致病力会产生影响, 且不同种类、同一种类的不同品系之间存在差异。
经UV-B辐射后, 供试昆虫病原线虫引起全部寄主昆虫死亡时间发生变化。致病力升高的品系, 其引起全部寄主昆虫死亡的时间缩短, 包括S. felitiae 0639C和S. felitiae 0663TD; 而致病力降低的品系, 使寄主昆虫全部死亡的时间增长, 如S. felitiae 0661YM和S. felitiae 0619HT品系、S. kraussei 0663HT和S. kraussei 0657L品系及H. megidis 0641TY和H. brevicaudis 0627M品系; 致病力未发生变化的品系, 其使寄主昆虫全部死亡的时间亦未发生显著变化, 如S. felitiae 0622L。说明UV-B辐射对昆虫病原线虫致病力的影响, 不但包括毒力大小的影响, 同时也影响了其对寄主的致死速率。
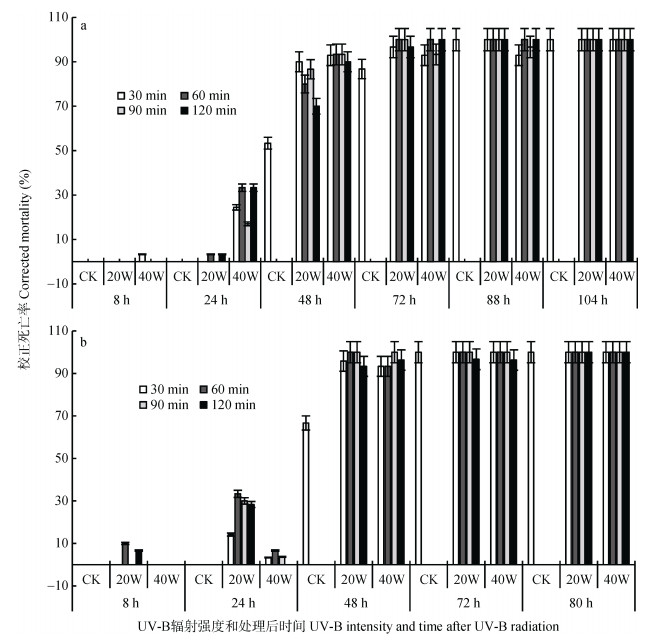
2.3 不同UV-B辐射强度及时长对Steinernema felitiae 0639C和0663TD致病力的影响图 1表明, 与对照相比, S. felitiae 0663TD和S. felitiae 0639C在20 W和40 W UV-B辐射30 min、60 min、90 min、120 min后, 引起寄主昆虫死亡的时间发生变化, 其中S. felitiae 0639C随着辐射强度的增大引起寄主昆虫开始死亡时间提前, 而S. felitiae 0663TD随着辐射强度增加, 引起寄主昆虫开始死亡时间延后; 不同紫外辐射时长对S. felitiae 0663TD和S. felitiae 0639C致病力无影响, 30 min、60 min、90 min、120 min辐射处理之间差异不显著(P > 0.05)。
|
图 1 UV-B辐射强度与处理时间对处理后不同时间S. felitiae 0639C(a)和0663TD(b)致病力的影响 Fig. 1 Effects of UV-B radiation time and intensity on pathogenicity of S. felitiae 0639C (a) and 0663TD (b) after different times of treatment |
从图 1a可知, 40 W UV-B辐射处理的S. felitiae 0639C线虫, 侵染8 h后引起寄主昆虫的死亡, 而经20 W辐射处理则侵染后24 h引起寄主昆虫死亡, 对照组在两个时间点均未引起寄主昆虫死亡; 侵染24 h时, 40 W辐射处理的线虫致病力显著高于20 W和对照(P < 0.05), 48 h时两种辐射强度处理的线虫引起寄主昆虫的累计死亡率之间差异不显著(P > 0.05)。不同的紫外辐射时长后, S. felitiae 0639C品系对大蜡螟的致病力无显著变化。
S. felitiae 0663TD线虫在经20 W UV-B辐射后, 侵染8 h后就可引起寄主昆虫的死亡, 而经40 W辐射处理的线虫, 侵染后24 h引起寄主昆虫的死亡, 对照组在此两个时间点均未引起寄主昆虫死亡, 且24 h时20 W辐射预处理后的线虫致病力显著高于40 W和对照组(P < 0.05), 48 h后两种辐射强度处理后的线虫引起寄主昆虫的累计死亡率之间差异不显著(P > 0.05);不同的紫外辐射时长后, S. felitiae 0663TD品系对大蜡螟的致病力无显著变化。
综上所述, 紫外辐射能刺激S. felitiae 0663TD和S. felitiae 0639C侵染和致死寄主昆虫, 侵染前期(24 h)紫外辐射强度对S. felitiae 0663TD和S. felitiae 0639C的致病力有影响, 随着UV-B辐射强度的增加, 处理强度(20W和40 W)对S. felitiae 0663TD和S. felitiae 0639C的致病力无影响; 一定的辐射时长内(120 min), 辐射时长对S. felitiae 0663TD和S. felitiae 0639C的致病力无影响。
3 讨论与结论全球环境与气候对臭氧层产生显著影响, 而臭氧层的破坏使地球表面的UV-B辐射不断增强, 地球上的生物也将面临逐渐增强的UV-B胁迫, 因此揭示UV-B胁迫对生命体的影响具有重要意义。以往研究结果表明, 平流层O3的耗损及由此导致的太阳UV-B辐射强度的增加, 对生活在地球生物圈中的各种生物及其生存环境质量都会产生影响, 成年节肢动物的存活时间和逆境压力的强度、时长之间存在着明显的相关性, 但是自然种群在生境中的相关研究鲜见报道[11-12]。UV-B辐射增强对节肢动物或昆虫的影响也有相关报道[13-14], 而UV-B辐射对昆虫病原线虫的影响相关报道较少。
昆虫病原线虫作为一种生命体, 逆境胁迫对其最明显的影响是对生物学特性的影响, 研究表明其存活率、侵入率、致病力和生殖力在受到逆境胁迫时都会发生变化[8-10]。且不同种或同一种类的不同品系昆虫病原线虫在不同发育阶段, 对不良环境条件的抵御能力均不同[8-10]。线虫的整个生活史中, 最能抵御逆境压力的阶段为抗逆性幼虫daner juvenile (侵染期线虫), 逆境对昆虫病原线虫侵染期线虫的影响及塑造, 直接决定了线虫是否能经过逆境条件进入下一个生活史阶段[1]。甘肃省大部分地区处于500 mm等雨量线以下, 总体气候特征为干旱, 且夏季降水集中, 占年降水的70%左右, 造成了干旱缺雨、夏季日照时数长、紫外辐射强度大的地理气候大背景。项目组在前期的研究中发现, 甘肃省(跨古北区和东洋区)昆虫病原线虫资源比较丰富(8种51个品系, 其中4种属中国新记录种)。本研究表明, UV-B辐射对甘肃省诱集分离得到的昆虫病原线虫存活有影响, 但是在一定的胁迫强度和时长内, 大部分侵染期线虫能存活并完成生活史, 说明甘肃省昆虫病原线虫对当地强UV-B辐射胁迫有一定的适应性和抗逆性。
本研究表明, 不同昆虫病原线虫和同种不同品系昆虫病原线虫受不同逆境胁迫后, 其致病力的变化不同, 这与以往的研究结果相一致。分析其原因, 首先昆虫病原线虫对逆境胁迫的不同耐受程度首先取决于其遗传特性, 不同种、同种不同品系线虫对同种胁迫表现不同的耐受水平; 其次, 同一种线虫在对不同生存环境的长期适应中, 抗逆能力也会发生较大的变化以获得与生境相适应的特性[8-10, 20]。本研究所用不同昆虫病原线虫品系, 为甘肃省不同地区或不同生境中诱集分离得到。不同的地理环境和气候条件、非生物胁迫及当地作物栽培管理制度、适宜寄主昆虫等因素, 均可导致不同品系的线虫对紫外辐射的抗逆性和适应性发生分化, 从而使其经辐射后对大蜡螟的致病力发生不同变化。
昆虫病原线虫对隐蔽性害虫具有较高的防治效果, 但是对叶面害虫的防治效果较低, 其中一个重要的原因就是UV-B辐射对侵染期线虫的影响[8-10]。本研究结果表明, UV-B辐射在一定的辐射时间内, 对甘肃省昆虫病原线虫的存活率无显著影响, 说明甘肃省土著昆虫病原线虫对UV-B辐射有一定的抗逆性, 为甘肃省昆虫病原线虫对叶部害虫的防治及推广提供了理论依据。
决定昆虫病原线虫对寄主昆虫的控制效能的因素, 除昆虫病原线虫自身毒力大小外, 还与其行为特征有关, 如寄主搜寻能力和迁移能力。昆虫病原线虫对叶面害虫或其他裸露性害虫的控制效能较低, 部分文献推测, 是因为紫外辐射降低了昆虫病原线虫的毒力[8-9]。但本研究表明, 经UV-B辐射后, 有2个品系的昆虫病原线虫的致病力升高, 充分说明紫外辐射有刺激昆虫病原线虫侵染和致死寄主昆虫的作用, 同时也说明UV-B辐射降低昆虫病原线虫对叶部害虫的防治效果, 主要因素不是因为存活率和致病力的下降, 而是其他原因造成的。根据现有的研究结果推测, 其中一个重要的原因应为UV-B辐射对昆虫病原线虫的迁移能力及趋性造成影响, 在后期可进行进一步的研究。
不同线虫品系的致病力大小和其能量储备量有关[10]。亦有研究表明, 昆虫病原线虫的能量物质是决定昆虫行为特征和对逆境响应的基础[8-9], 关于UV-B辐射对昆虫病原线虫体内能量物质的影响, 及能量物质对致病力的影响是否取决于能量物质对其侵染行为和迁移能力的调控, 将在后期继续探讨。
本研究表明, 甘肃省昆虫病原线虫对紫外辐射有一定耐受能力和适应性。在20 W和40 W强度下, 短时间UV-B辐射对昆虫病原线虫N存活率无显著影响, 但随辐射强度增加, 其存活率会下降。经一定强度的紫外辐射后, 9个甘肃省土著昆虫病原线虫品系的致病力存在差异、同一种的不同品系之间, 其致病力变化不同。在20W UV-B辐射30 min后, 斯氏S. felitiae 0639C的致病力显著升高(P < 0.05), S. felitiae 0661YM的致病力显著降低(P < 0.05), 其余供试品系致病力变化差异均不显著(P > 0.05)。
UV-B辐射对昆虫病原线虫致病力的影响, 不但包括毒力大小的影响, 同时也影响了其对寄主的致死速率。经UV-B辐射后, 供试昆虫病原线虫引起全部寄主昆虫死亡时间发生变化。致病力升高的品系, 其引起全部寄主昆虫死亡的时间缩短; 而致病力降低的品系, 使寄主昆虫全部死亡的时间增长; 致病力未发生变化的品系, 其使寄主昆虫全部死亡的时间亦未发生显著变化。
紫外辐射能刺激S. felitiae 0663TD和S. felitiae 0639C侵染和致死寄主昆虫, 不同强度UV-B辐射对S. felitiae 0663TD和S. felitiae 0639C引起寄主昆虫死亡的时间有影响。经辐射预处理后, 2品系线虫引起寄主昆虫死亡的时间较对照组均提前, 其中S. felitiae 0639C随着辐射强度的增大, 引起寄主昆虫开始死亡时间提前, 而S. felitiae 0663TD随着辐射强度增加, 引起寄主昆虫开始死亡时间延后。
侵染前期(24 h)紫外辐射强度对S. felitiae 0663TD和S. felitiae 0639C的致病力有影响, 随着UV-B辐射强度的增加, S. felitiae 0639C致病力升高, 而S. felitiae 0663TD致病力降低(仍高于未辐射组), 但随着时间的推移(48 h后), 辐射强度(20 W和40 W)对S. felitiae 0663TD和S. felitiae 0639C的致病力无影响; 一定的辐射时长内(120 min), 辐射时长对S. felitiae 0663TD和S. felitiae 0639C的致病力无影响。
| [1] |
GAUGLER R. Entomopathogenic Nematodes[M]. Wallingford, UK: CAB International, 2002: 1-13.
|
| [2] |
CUTHBERTSON A G S, AUDSLEY N. Further screening of entomopathogenic fungi and nematodes as control agents for Drosophila suzukii[J]. Insects, 2016, 7(2): 24. DOI:10.3390/insects7020024 |
| [3] |
ILAN T, KIM-SHAPIRO D B, BOCK C H, et al. Magnetic and electric fields induce directional responses in Steinernema carpocapsae[J]. International Journal for Parasitology, 2013, 43(10): 781-784. DOI:10.1016/j.ijpara.2013.05.007 |
| [4] |
KAPLAN F, ALBORN H T, VON REUSS S H, et al. Interspecific nematode signals regulate dispersal behavior[J]. PLoS One, 2012, 7(2): e38735. |
| [5] |
KASPI R, ROSS A, HODSON A K, et al. Foraging efficacy of the entomopathogenic nematode Steinernema riobrave in different soil types from California citrus groves[J]. Applied Soil Ecology, 2010, 45(3): 243-253. DOI:10.1016/j.apsoil.2010.04.012 |
| [6] |
SHAPIRO-ILAN D I, HAN R, DOLINSKI C. Entomopathogenic nematode production and application technology[J]. Journal of Nematology, 2012, 44(2): 206-217. |
| [7] |
WILLETT D S, ALBORN H T, STELINSKI L L. Multitrophic effects of belowground parasitoid learning[J]. Nature Scientific Reports, 2017, 7(1): 2067. DOI:10.1038/s41598-017-02193-2 |
| [8] |
曹翠玲, 刘倩, 简恒, 等. 昆虫病原线虫对非生物胁迫的响应机制[J]. 昆虫学报, 2009, 52(3): 312-318. CAO C L, LIU Q, JIAN H, et al. Response mechanisms of entomopathogenic nematode to abiotic stress[J]. Acta Entomologica Sinica, 2009, 52(3): 312-318. DOI:10.3321/j.issn:0454-6296.2009.03.011 |
| [9] |
钱秀娟.甘肃省昆虫病原线虫资源及其对非生物胁迫的适应性研究[D].兰州: 甘肃农业大学, 2014: 29-50 QIAN X J. Entomopathogenic nematodes resources of Gansu Province and its adaptation to abiotic stress[D]. Lanzhou: Gansu Agricultural University, 2014: 29-50 |
| [10] |
SHAPIRO-ILAN D I, BROWN I, LEWIS E E. Freezing and desiccation tolerance in entomopathogenic nematodes:Diversity and correlation of traits[J]. Journal of Nematology, 2014, 46(1): 27-34. |
| [11] |
胡祖庆, 亢菊侠, 赵惠燕, 等. 不同紫外(UV-B)辐射时间对两种体色型麦长管蚜后代生物学特征的影响[J]. 生态学报, 2010, 30(7): 1812-1816. HU Z Q, KANG J X, ZHAO H Y, et al. Effect of UV-B radiation on biological characteristics of two body color biotypes of Sitobion apenae (Fab.) offspring[J]. Acta Ecologica Sinica, 2010, 30(7): 1812-1816. |
| [12] |
闫生荣, 周青. 紫外辐射与复合胁迫对植物抗氧化酶系统的影响[J]. 中国生态农业学报, 2007, 15(3): 195-197. YAN S R, ZHOU Q. Effects of supplementary UV-B radiation and combined stresses on plant antioxidant enzymes[J]. Chinese Journal of Eco-Agriculture, 2007, 15(3): 195-197. |
| [13] |
杜军利, 吴德功, 张廷伟, 等. 紫外线(UV-B)辐射对不同色型豌豆蚜生物学特性的影响[J]. 中国生态农业学报, 2012, 20(12): 1626-1630. DU J L, WU D G, ZHANG T W, et al. Effects of UV-B radiation on biological characteristics of different color pea aphid morphs (Acyrthosiphon pisum)[J]. Chinese Journal of Eco-Agriculture, 2012, 20(12): 1626-1630. |
| [14] |
唐莉娜, 林文雄, 梁义元, 等. UV-B辐射增强对水稻蛋白质及核酸的影响研究[J]. 中国生态农业学报, 2004, 12(1): 40-42. TANG L N, LIN W X, LIANG Y Y, et al. Effects of enhanced ultraviolet-B radiation on soluble protein and nucleic acid in rice leaves[J]. Chinese Journal of Eco-Agriculture, 2004, 12(1): 40-42. |
| [15] |
ZHAO Y L, WANG D Y. Formation and regulation of adaptive response in nematode Caenorhabditis elegans[J]. Oxidative Medicine and Cellular Longevity, 2012, 2012: 564093. |
| [16] |
钱秀娟, 谷黎娜, 邢玉芳, 等. 甘肃省昆虫病原线虫区系研究[J]. 草地学报, 2014, 22(3): 593-599. QIAN X J, GU L N, XING Y F, et al. Occurrence of entomopathogenic nematodes in Gansu Province[J]. Acta Agrestia Sinica, 2014, 22(3): 593-599. |
| [17] |
钱秀娟, 刘长仲, 阮艳娥. 昆虫病原线虫对甘肃省草地蛴螬的致病力研究[J]. 草地学报, 2015, 23(2): 414-421. QIAN X J, LIU C Z, RUAN Y E. Pathogenicity of entomopathogenic nematodes to grass grubs (Coleoptera:Scarabaeidae)[J]. Acta Agrestia Sinica, 2015, 23(2): 414-421. |
| [18] |
QIAN X J, GU L N, XING Y F, et al. Entomopathogenic nematodes isolated from Gansu province and four new species in China[J]. Applied Mechanics and Materials, 2014, 651/653: 328-336. DOI:10.4028/www.scientific.net/AMM.651-653 |
| [19] |
谷黎娜, 钱秀娟, 刘长仲. 甘肃省昆虫病原线虫3个优良品系的生物学特性研究[J]. 甘肃农业大学学报, 2009, 44(2): 85-89. GU L N, QIAN X J, LIU C Z. Biological characteristics of three fine strains of insect pathogenic nematode in Gansu Province[J]. Journal of Gansu Agricultural University, 2009, 44(2): 85-89. DOI:10.3969/j.issn.1003-4315.2009.02.018 |
| [20] |
GREWAL P S, BORNSTEIN-FORST S, BURNELL A M, et al. Physiological, genetic, and molecular mechanisms of chemoreception, thermobiosis, and anhydrobiosis in entomopathogenic nematodes[J]. Biological Control, 2006, 38(1): 54-65. DOI:10.1016/j.biocontrol.2005.09.004 |
 2019, Vol. 27
2019, Vol. 27



